优化PROTAC的新策略:可逆共价
注:文末有研究团队简介及本文科研思路分析
靶向蛋白水解的嵌合体(Proteolysis targeting chimera,PROTAC)是基于泛素-蛋白酶解系统而发展的一种通过小分子化合物来诱导实现靶蛋白降解的新技术。PROTAC概念由Crews在2001年 提出,最初基于多肽段的PROTAC,分子量大,活性低,其应用前景并不被看好。2008年,完全基于小分子的PROTAC问世,再一次引起人们关注,遗憾的是其活性仍然停留在微摩尔级。直至2015年,基于E3连接酶VHL和CRBN的PROATC相继被报道,其活性也终于达到了纳摩尔级。至此,PROTAC技术进入了蓬勃发展期,其在靶向“不可成药”靶点和克服耐药性方面展现出了巨大的潜力,引发了学术界和工业界的极大兴趣。PROTAC作为一类双功能小分子,可以同时结合靶向蛋白与E3 连接酶,促使形成非常重要的三元复合物,随之将泛素分子标记到靶向蛋白质上,然后通过泛素-蛋白酶解系统将靶向蛋白降解。区别于传统的小分子药物作用机制,PROTAC最大特点在于其诱导蛋白降解后可以重复利用,即“催化”特性。另一方面,PROTAC较大的分子量(~1000 Da)也造成其透膜性和在细胞内的累积较差,从而一定程度上制约其活性。
日前,来自美国贝勒医学院的王津课题组在Nature Communications上报道了一类结构新颖的基于可逆共价反应的PROTAC分子,来靶向降解布鲁顿氏酪氨酸激酶(Bruton's tyrosine kinase, BTK)。在研究过程中作者意外发现这类可逆共价PROTAC分子可以显著提高其在细胞内的累积和靶向参与作用,同时发挥抑制剂和降解剂的双重功能。其独特的氰基丙烯酰胺基团,使PROTAC分子在增加与靶向蛋白结合力的同时,继续保留着PROTA的“催化”特性(图1),可谓一举双得。
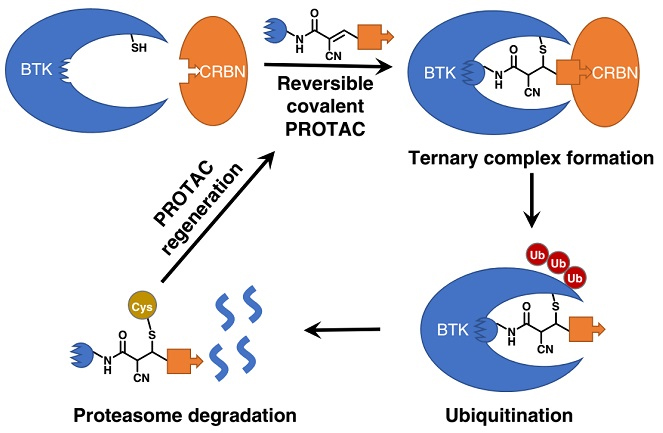
图1. 可逆共价PROTAC作用机制
该课题的初衷是基于不同类型的BTK弹头设计PROTAC,如:可逆共价(Reversible Covalent, RC)、可逆非共价(Reversible Noncovalent, RNC)以及不可逆共价(Irreversible Covalent, IRC),来进一步考察其对BTK的降解效率及作用机制。研究结果表明,可逆共价的RC-1,相比可逆非共价的RNC-1 和不可逆共价的IRC-1,无论在蛋白降解还是抑制细胞生长方面,都有着显著的优势(图2)。
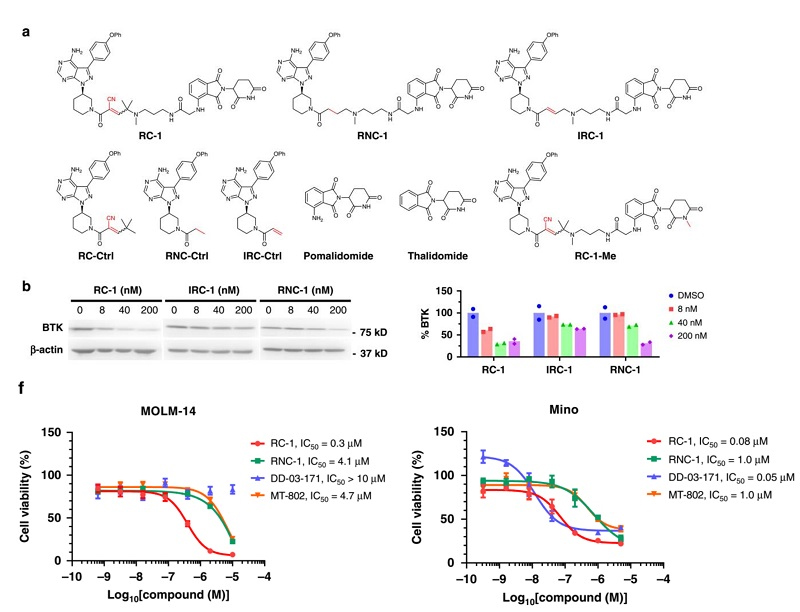
图2. PROTAC 诱导BTK降解和抑制肿瘤细胞生长
蛋白组学分析显示,可逆共价的RC-1对蛋白降解有着更高的选择性(图3)。而在诱导形成BTK-PROTAC-CRBN三元复合物方面,RC-1也能够更加高效地形成稳定的三元复合物。

图3. 蛋白组学分析蛋白降解
进一步,作者在比较不同类型PROTAC分子在细胞内的BTK和CRBN靶向参与作用(target engagement)时发现,RC-1由于其可逆共价的特性,在BTK和CRBN靶向参与作用方面都有着显著的优势,其BTK靶向参与作用与其弹头RC-Ctrl旗鼓相当(59 nM vs 47 nM)(图4)。为了比较不同PROTAC在细胞内的累积程度,作者创造性地定义了细胞内相对药物累积系数。结果表明, RC-1在细胞内的累积远高于RNC-1和IRC-1,这也是造成RC-1在急性髓系白血病细胞系MOLM-14中毒性显著强于RNC-1和IRC-1的主要原因。
此外,RC-1同样可以有效降解突变型BTK(C481S),意味着其有客服耐药性的潜力。与此同时,RC-1在小鼠体内展现了较好的代谢稳定性(血浆半衰期为3.4小时),并且,能够显著降低小鼠体内BTK水平,这为该药物进行后续的体内研究甚至临床研究提供了可能。
更为重要是,作者成功将“引入可逆共价基团来增强PROTAC在细胞内的累积和靶向参与作用”这一策略推广到其他的靶向蛋白,如FLT3(图4)。这为PROTAC的发展开辟了一个新的方向。
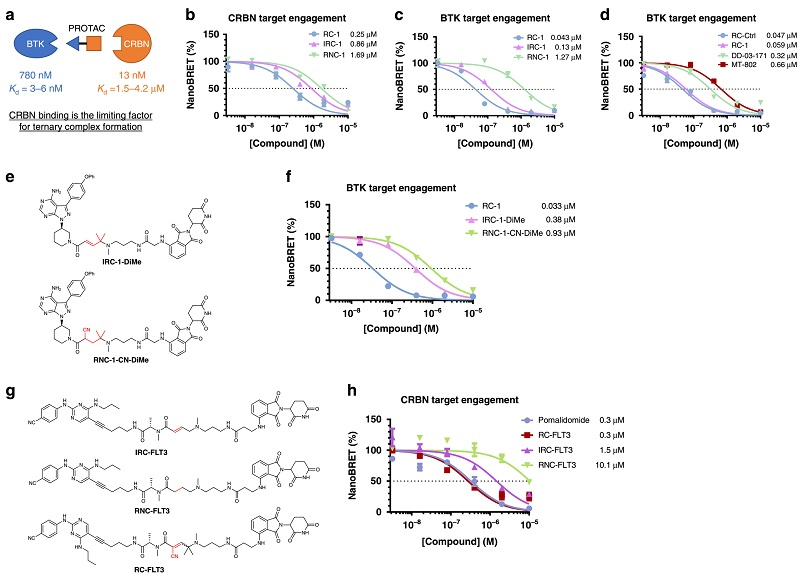
图4. PROTAC分子在细胞内的靶向参与作用
以上成果由郭文豪博士和亓晓丽博士共同完成,王津为通讯作者。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Enhancing intracellular accumulation and target engagement of PROTACs with reversible covalent chemistry
Wen-Hao Guo, Xiaoli Qi, Xin Yu, Yang Liu, Chan-I Chung, Fang Bai, Xingcheng Lin, Dong Lu, Lingfei Wang, Jianwei Chen, Lynn Hsiao Su, Krystle J. Nomie, Feng Li, Meng C. Wang, Xiaokun Shu, José N. Onuchic, Jennifer A. Woyach, Michael L. Wang, Jin Wang
Nat. Commun., 2020, 11, 4268, DOI: 10.1038/s41467-020-17997-6
王津博士介绍
王津,美国贝勒医学院药理学和化学生物学系副教授。2003年本科毕业于北京大学,2007年于俄亥俄州立大学取得博士学位,随后在北卡罗来纳大学教堂山校区进行博士后研究,2011年起就职于贝勒医学院。研究兴趣集中在可转化的科研领域,包括新型荧光探针,小分子药物,抗体药物偶联(ADC),蛋白以及代谢组学(proteomics and metabolomics)。课题组发展的可定量的谷胱甘肽荧光探针被世界100多个课题组应用。在相关领域已发表多篇具有影响力的论文,包括Nature Communications、PNAS、JACS、ACS Chemical Biology 等。
贝勒医学院王津课题组目前有多个化学和生物博士后位置以及技术员位置开放,详情请见:
https://www.x-mol.com/news/464802
科研思路分析
Q:这项研究最初是什么目的?或者说想法是怎么产生的?
A:正如上面所述,这项研究的最初目的是想发展基于可逆共价的PROTAC,并且比较其与可逆非共价和不可逆共价的PROTAC对靶向蛋白的降解效率和作用机制。基于我们组之前发展的大量可逆共价GSH荧光探针,我们认为可逆共价的PROTAC对靶向蛋白不但有着较强的结合力,而且在蛋白降解之后,PROTAC分子可以释放出来重新利用。
Q:研究过程中遇到哪些挑战?
A:研究中遇到最大的挑战是如何有效比较不同PROTAC分子在细胞内的浓度。我们尝试过用LC-MS定量,但是由于PROTAC分子的特殊性,其很容易粘附在膜上,而无法获得真正细胞内的PROTAC浓度。最终,我们利用Promega发展的基于NanoBRET的靶向蛋白参与作用竞争实验来比较不同类型PROTAC的靶向参与作用。并且,定义了细胞内相对药物累积系数,从而可以很好地比较不同PROTAC在细胞内的浓度与累积。
Q:该研究成果可能有哪些重要的应用?哪些领域的企业或研究机构可能从该成果中获得帮助?
A:从学术角度来讲,我们发现“引入可逆共价基团来增强PROTAC在细胞内的累积和靶向参与作用”这一策略具有普遍性,可以被应用于发展靶向其他蛋白的PROTAC。这也为如何能够进一步优化PROTAC效能提供了一个新的方向。近年来,各大药企也都在致力发展PROTAC技术,相信我们的研究同样可以为药企在研发PROTAC药物时提供一个新的借鉴方向,从而能够获得最佳的临床候选PROTAC分子。
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!


























 京公网安备 11010802027423号
京公网安备 11010802027423号