手性光催化剂辅助的丙二烯去外消旋化
去外消旋化反应是指外消旋体在降低一种对映体数量的同时增加另一种对映体数量,从而使外消旋体形成单一对映体的过程。在溶液中实现去外消旋化的方法有数种,但它们要么依赖非手性中间体,要么依赖化学计量的手性试剂。如果去外消旋化是在催化下进行的,则需要能量对相关的熵损失进行补偿。近年来,光化学为这一挑战提供了解决方案(图1,J. Am. Chem. Soc., 1968, 90, 2957-2958; J. Am. Chem. Soc., 1973, 95, 8472-8474; Tetrahedron Lett., 1973, 14, 4159-4162; Angew. Chem. Int. Ed., 2020, 59, 4998-5001; Nature, 2018, 564, 197-199),即手性光催化剂通过非共价结合的方式来区分化合物的两种对映体形式。其中与催化剂结合的对映体通过敏化作用被激发,随后通过非手性中间体进行外消旋化。理想情况下,催化剂只能与其中一种对映体相互作用,因此非结合对映体在溶液中的含量越来越多,最终得到单一的对映体。然而,实际情况中,催化剂与对映体的结合情况并不是那么完美,其它参数也可能会影响选择性。
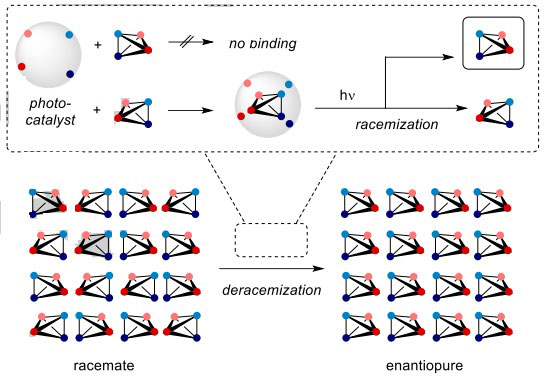
图1. 光催化剂去消旋化反应简图。图片来源:Angew. Chem. Int. Ed.
2018年,德国慕尼黑工业大学的Thorsten Bach(点击查看介绍)课题组报道了在可见光的催化下,利用手性光敏剂实现了含六元内酰胺的丙二烯的去外消旋化(Nature, 2018, 564, 240-243),但是反应的底物范围比较局限。于是,作者设想能否将去外消旋化的范围扩展到其它类型的丙二烯并进行后续的转化?最近,他们在可见光(λ= 420 nm)和三重态光敏剂(2.5 mol%)的作用下,通过氢键选择性地识别丙二烯对映体,实现了含五元内酰胺的三取代丙二烯的去外消旋化,并且丙二烯的轴手性可通过Diels-Alder反应或溴化反应有效地传递到点手性(手性中心)。相关成果发表于Angew. Chem. Int. Ed. 期刊上。
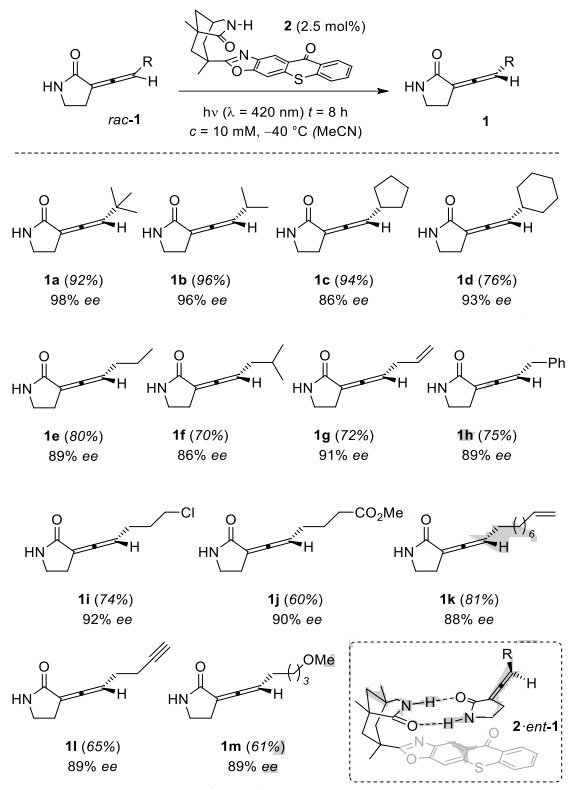
图2. 底物的范围。图片来源:Angew. Chem. Int. Ed.
外消旋的丙二烯rac-1由N-对甲氧基苄基(PMB)吡咯烷酮经α-碘化、形成三苯基膦盐、Wittig反应和脱保护四步反应制备而成(图2),该类化合物在室温下稳定,但在酸性条件下会有部分分解。鉴于硫杂蒽酮2在电磁波谱的可见光部分具有明显的吸收,且丙二烯1a三重态能量ET = 268 kJ/mol(77 K, EtOH),硫杂蒽酮2的三重态能量为ET = 263 kJ/mol(77 K, PhCF3),这表明2可用于丙二烯的去外消旋化。随后,作者对反应条件进行优化,得到最佳的反应条件:外消旋丙二烯rac-1在可见光(λ= 420 nm)、三重态光敏剂(2.5 mol%)以及乙腈中于-40 ℃下反应8 h。
在最优条件下,作者考察了反应的底物范围(图2),结果显示三取代丙二烯衍生物(1a-1m)的ee 值可达86% - 98%,并且根据随后的反应确定出产物的绝对构型。该反应对烯基、苯基、氯、酯基、炔基和甲氧基(1g-1m)等官能团耐受性较好,尽管在纯化过程中丙二烯的不稳定性影响了部分产率,但在光照过程中未发现分解现象。
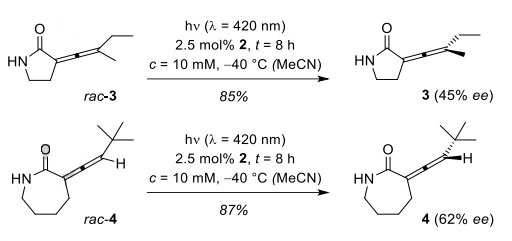
图3. 底物的进一步拓展。图片来源:Angew. Chem. Int. Ed.
为了进一步探索去外消旋化的底物范围,作者尝试在最优条件下考察四取代丙二烯rac-3的反应效果(图3),结果显示产物3的ee 值仅为45%,作者推测可能是由于甲基和乙基的大小差异使其与光敏剂2的键合程度有明显的区别。当使用柔韧性较高的七元内酰胺rac-4作为底物时,能以62%的ee 值得到部分去外消旋化产物4。
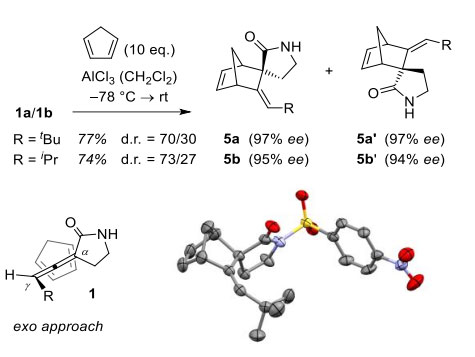
图4. 产物的后续反应。图片来源:Angew. Chem. Int. Ed.
接下来,作者选择简单易得的产物1a(98% ee)进行后续反应(图4)。对反应条件进行优化后,作者发现在低温Lewis酸催化下,1a与环戊二烯能够发生Diels-Alder反应,得到两个可以完全分离的非对映异构体5a和5a’。值得注意的是,环加成反应专一性地发生在丙二烯的α,β-不饱和双键而不是β,γ-不饱和双键。随后,用对硝基苯磺酰氯对产物进行处理,将所得的产物进行X-ray单晶衍射,结果和NOESY数据一致。随后,作者通过反常衍射确定了产物5a的绝对构型,反过来也证实了丙二烯1的绝对构型。事实上,Diels-Alder反应在三取代丙二烯较易接近的面(exo 面)上进行,并且有效地实现了轴手性向点手性的传递。有趣的是,产物5代表了一类重要的砌块,可以在多个位置进一步进行官能团化。

图5. 手性传递。图片来源:Angew. Chem. Int. Ed.
此外,将产物1a溶于CH2Cl2中与液溴反应,便能以较高的对映选择性(91% ee)得到二溴产物7(由NOESY数据确定相对构型),再次证实手性得到了有效的传递。具体的反应机理如下:溴先进攻远离叔丁基的α,β-不饱和双键,形成溴鎓离子6,随后被溴离子进攻,开环得到产物7。
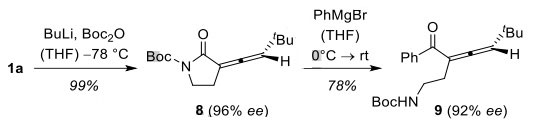
图6. 内酰胺的开环。图片来源:Angew. Chem. Int. Ed.
最后,作者对吡咯烷酮环的开环过程和丙二烯的立体化学完整性进行了研究。为了避免氮原子上酸性质子的影响,首先要安装保护基,对反应条件进行优化后,用叔丁氧羰基(Boc)对其进行保护。鉴于N-Boc保护的内酰胺8在亲核试剂的作用下可能会发生开环反应,因此作者选择苯基溴化镁作为亲核试剂,最终以78%的收率和92%的ee 值得到了期望的三取代丙二烯产物9。尽管在此过程中ee 值有所下降,但 在某种程度上,仍能用于立体选择性的合成中。
总结
Thorsten Bach课题组发展了一种可见光介导的三取代丙二烯类化合物的去外消旋化反应,该反应具有较高的对映选择性(86%-98% ee),并且在后续的转化中能有效地将轴手性传递到点手性。此外,四取代丙二烯、含七元内酰胺环的丙二烯也能实现去外消旋化,为丙二烯类化合物的去外消旋化提供了一条高效、简便的方法。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Photochemical Deracemization of Allenes and Subsequent Chirality Transfer
Manuel Plaza, Christian Jandl, Thorsten Bach
Angew. Chem. Int. Ed., 2020, DOI: 10.1002/anie.202004797
导师介绍
Thorsten Bach
https://www.x-mol.com/university/faculty/2367
(本文由有所不为供稿)
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!


























 京公网安备 11010802027423号
京公网安备 11010802027423号