ACS Catal.:手性α-氨基硼酸衍生物的不对称催化氢化合成
有机硼化合物具有特殊的物理和化学性质,因而被广泛应用于化学试剂合成和医药研发领域。其中,作为手性氨基酸类似物的手性α-氨基硼酸更是得到了药物、生物和有机化学家们的广泛关注。手性α-氨基硼酸是众多上市以及在研药物的重要结构片段,代表性药物包括用于治疗多发性骨髓瘤和套细胞淋巴瘤的Bortezomib(Velcade®)及其第二代药物Ixazomib(Ninlaro®)和Delanzomib等(图1)。目前,研究含有手性α-氨基硼酸(酯)结构的活性分子依然是药物化学领域的热点。

图1. 含有手性α-氨基硼酸结构的药物及活性分子
合成手性α-氨基硼的传统方法包括:手性辅基法和不对称锂-硼化法;不对称催化的方法包括:亚胺和烯胺的不对称硼化法、烯基硼化合物的不对称胺化法等(图2)。这些方法因其效率低、环境不友好、原子经济性欠佳等缺点限制了其在工业化上的应用。过渡金属催化的不对称氢化因其具有高效、绿色等优点而被认为是最具工业化前景的方法之一。然而,用不对称氢化的方法合成手性α-氨基硼的研究至今未有报道,其挑战在于获得高的立体选择性的同时还要在氢化还原和氢解脱硼中获得高的化学选择性。

图2. 合成手性α-氨基硼酸衍生物的不对称催化方法
上海交通大学张万斌(点击查看介绍)课题组长期致力于过渡金属催化的不对称氢化研究(Chem. Rev., 2016, 116, 14769, Chin. J. Chem., 2018, 36, 443; Angew. Chem. Int. Ed., 2020, 59, 5371; Angew. Chem. Int. Ed., 2019, 58, 15767; Angew. Chem. Int. Ed., 2019, 58, 11505; Angew. Chem. Int. Ed., 2019, 58, 7329; Nature Commun., 2018, 9, 5000; Angew. Chem. Int. Ed., 2016, 55, 8444; Angew. Chem. Int. Ed., 2015, 54, 2260; Angew. Chem. Int. Ed., 2014, 53, 1901; Angew. Chem. Int. Ed., 2013, 52, 11632; Angew. Chem. Int. Ed., 2013, 52, 2203)。其中,以酰胺作为导向基团与双膦铑配合物作为催化剂实现了多种手性胺类化合物的高效合成(Angew. Chem. Int. Ed., 2019, 58, 11505; Chem. Commun., 2018, 54, 6024; Adv. Synth. Catal., 2018, 360, 2228; Chem. Eur. J., 2017, 23, 1040; Org. Lett., 2016, 18, 1290; Org. Lett., 2015, 17, 5380)。近期,该课题组报道了以双膦配体BenzP*的铑配合物为催化剂,对α-硼基烯酰胺进行不对称催化氢化以合成手性α-氨基硼衍生物的研究。相关研究发表于ACS Catalysis。
作者首先对底物导向基团的选取进行了研究(图3)。结果表明,当导向基团为五元的噁唑烷酮时,底物1a中BC-NC的扭转角为37.5°,N-C-O的角度为127.1°,同时O•••B键长为2.85 Å均大于1a-NH的理论计算值。而这些特点将有利于底物的C=C键和C=O键与催化剂中的过渡金属铑配位。
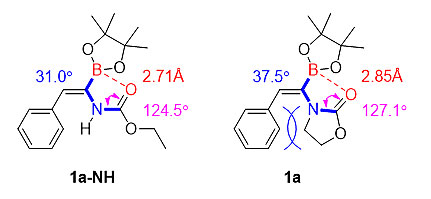
图3. 代表性底物
作者接着对氢化反应的条件进行了筛选和优化,发现当使用富电子的双膦配体BenzP*的铑配合物为催化剂和乙酸乙酯作为溶剂时,氢化反应的对映选择性和化学选择性最佳(图4)。
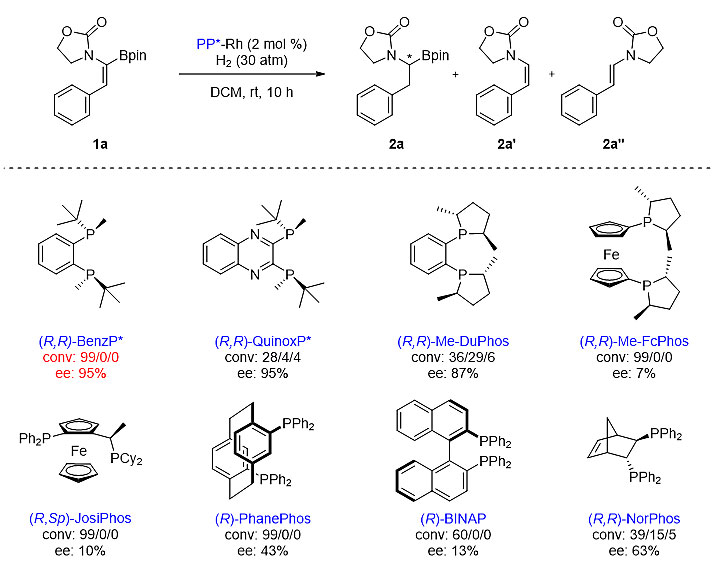

图4. 不对称催化的条件筛选与优化
作者在最优条件下考查了底物的适用范围(图5)。结果表明,具有不同取代基团的α-硼基烯酰胺底物均可高效转化为相应的手性的α-硼基胺衍生物,并获得最高99%的对映选择性。该反应可在克级规模进行,反应的活性和对映选择性均可保持。
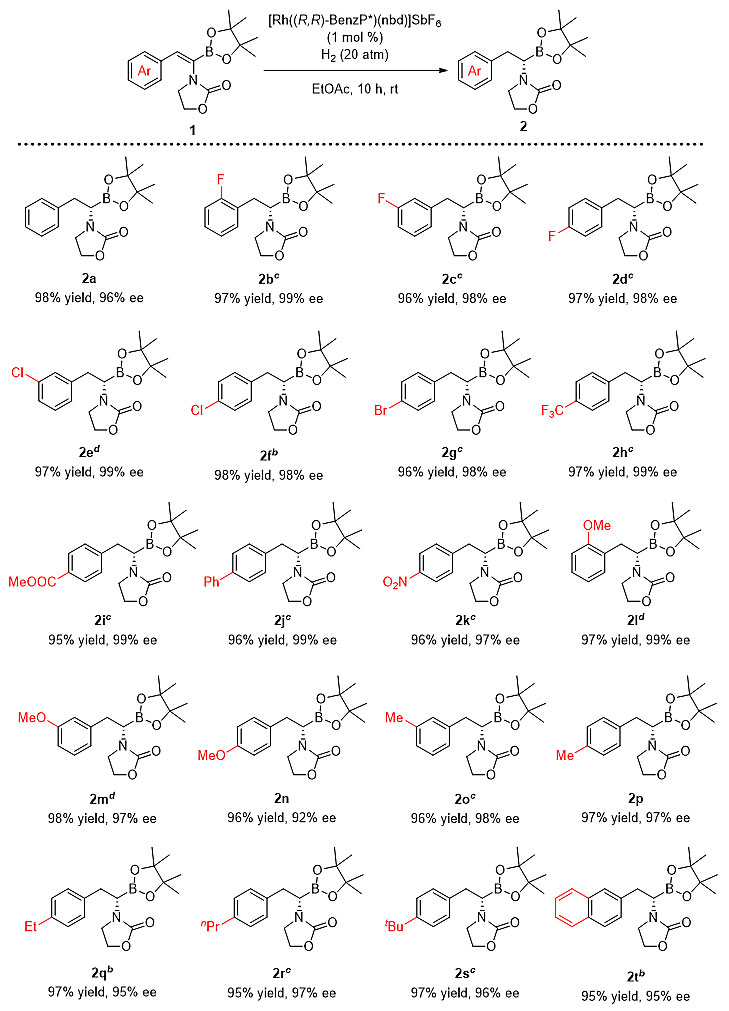
Conditions: 1 (0.1 mmol), [Rh((R,R)-BenzP*)(nbd)]SbF6(1 mol %), H2 (20 atm), EtOAc (2.0 mL), rt, 10 h, unlessotherwise noted. Isolatedyields. The ee values were determined by HPLCusing chiral columns. a[Rh((R,R)-BenzP*)(nbd)]SbF6 (2 mol %), 24 h. b24 h. c[Rh((R,R)-BenzP*)(nbd)]SbF6(4 mol %), 24 h.
图5. 底物范围
作者通过理论计算的方法推测了该催化反应的机理(图6)。在对映选择性控制步骤中,TS(S)的能垒差值远小于TS(R)的值,说明了S构型的产物为优势构型。同时,关键过渡态的优化结构显示,底物中的Bpin基团和配体BenzP*的叔丁基之间的相互作用是稳定优势过渡态的重要因素(图7)。
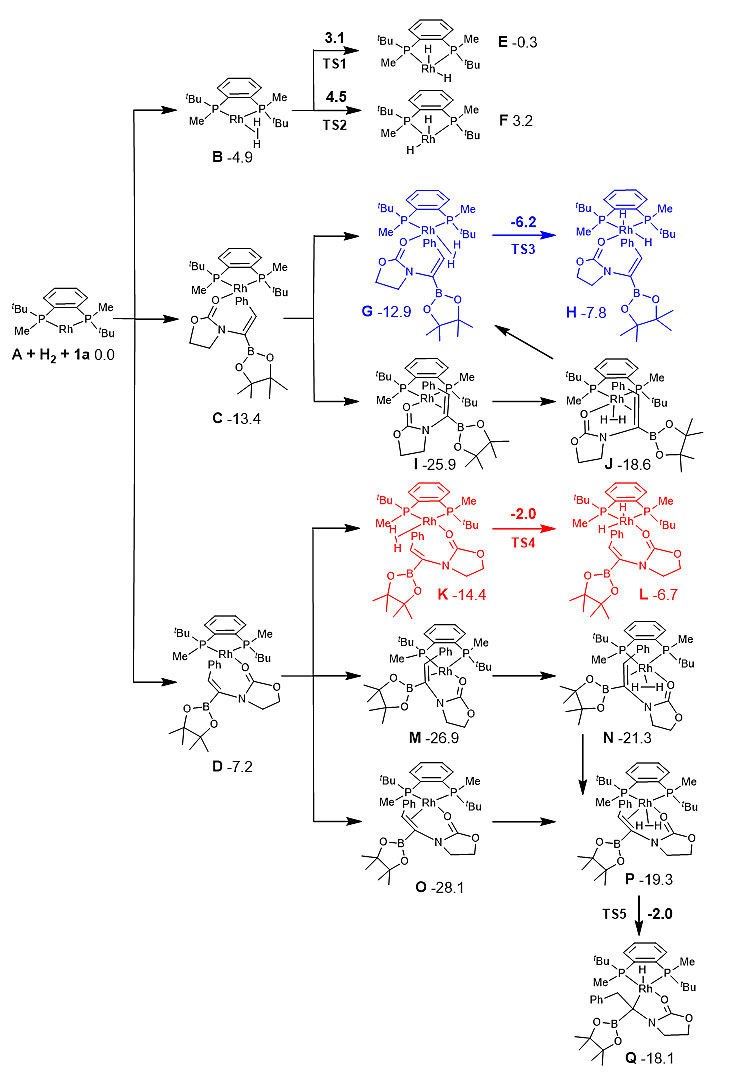
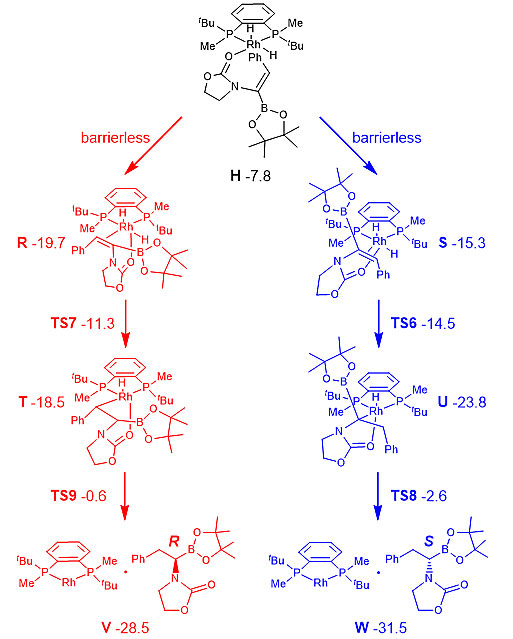
图6. 催化机理研究
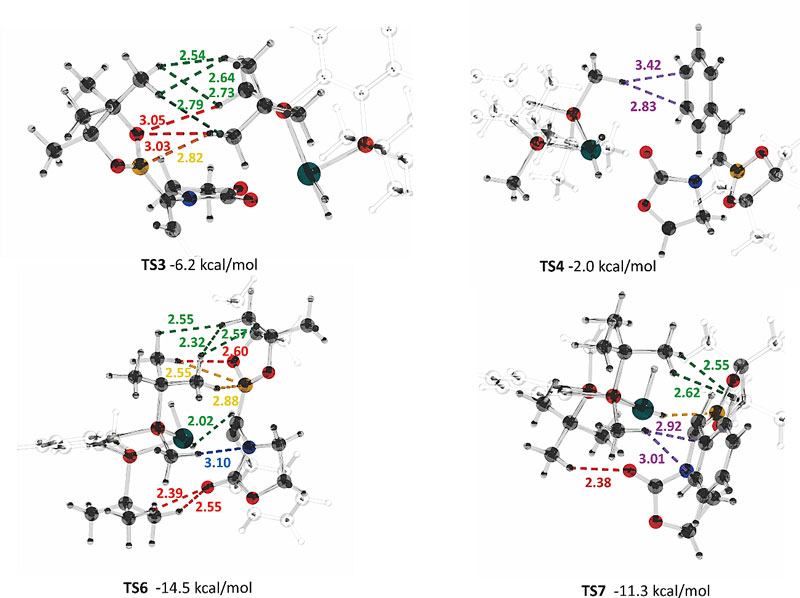
图7. TS3/TS4 (up)和TS6/TS7 (down)的优化结构
总结
上海交通大学张万斌课题组报道了双膦-铑催化的α-硼基烯酰胺的不对称氢化研究。通过底物中酰胺基团与铑的螯合配位作用以及底物的频哪醇硼酸酯与配体的叔丁基之间的非键相互作用,高对映选择性、高化学选择性地定量获得手性α-氨基硼酸酯。反应可达克级规模并且对映选择性可以保持。这一成果最近发表在ACS Catal.上,文章的第一作者是上海交通大学药学院博士生范冬阳。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Asymmetric Hydrogenation of α-Boryl Enamides Enabled by Nonbonding Interactions
Dongyang Fan, Jian Zhang, Yanhua Hu, Zhenfeng Zhang, Ilya D. Gridnev, Wanbin Zhang
ACS Catal., 2020, 10, 3232-3240, DOI: 10.1021/acscatal.9b04543
导师介绍
张万斌
https://www.x-mol.com/university/faculty/12592
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!



























 京公网安备 11010802027423号
京公网安备 11010802027423号