Angew内封面:青蒿素/(异)喹啉双剑合璧,抗击多重耐药性疟疾
恶性疟原虫曾是威胁人类生存的一类高致命真核类病原微生物。据世界卫生组织统计,在全世界恶性疟原虫每年约造成200多万人感染和100多万人死亡。目前临床所用的,有两类抗疟核心药物——青蒿素(ART,图1A)和喹啉衍生物(CQ,图1B)。青蒿素,是著名科学家、2015年诺贝尔生理或医学奖得主、共和国勋章获得者屠呦呦带领的团队从中国传统药用植物青蒿中提取的(本文介绍的论文原文特别强调“Dedicated to Professor Youyou Tu”)。喹啉和异喹啉,因其特有骨架,在临床上以不同商品药物形式对抗疟疾。
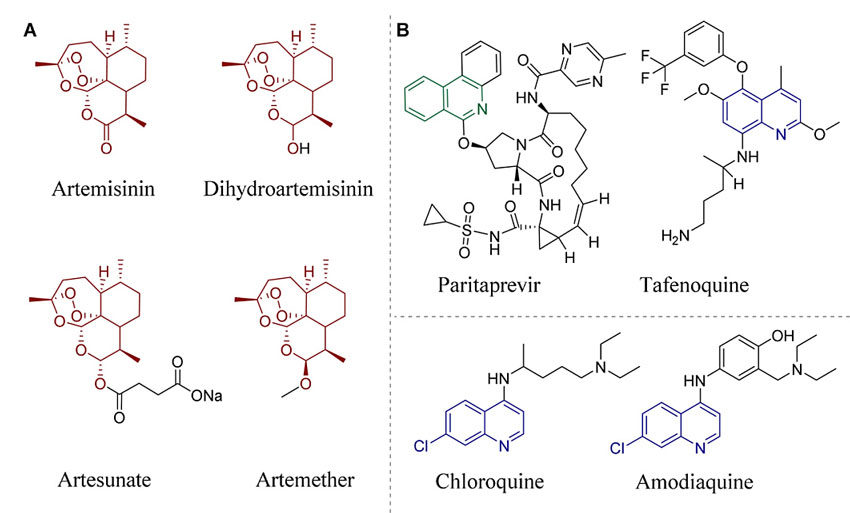
图1. A 青蒿素及其衍生物,B 喹啉衍生物。图片来源:Angew. Chem. Int. Ed.
令人担忧的是,近年来耐药性疟原虫呈现上升趋势。其中的两株代表性疟原虫Dd1和K1具有多重耐药性,耐喹啉、叶酸拮抗物、嘧啶胺、环胍等药物,包括青蒿素及其半合成衍生物也受到了这类耐药病原微生物威胁,这给疟疾治疗带来严峻的新挑战。为了应对耐药性,世界卫生组织推动基于青蒿素的多药物联合治疗,这其中就包括青蒿素和喹啉类药物的联合用药。既然青蒿素和(异)喹啉可以联合用药,那将两者核心骨架用化学方式键合成一个分子会不会治疗疟疾更有效呢?于是,有了青蒿素和(异)喹啉杂合式化合物的尝试(图2)。然而,对于这类“双核”式杂合分子的研究还处于初级阶段,特别是应用不同连接体构建杂合分子,系统探索结构-活性关系,鉴定杂合分子的潜在靶点,还未有报道。

图2. 青蒿素和奎宁杂合分子。图片来源:Angew. Chem. Int. Ed.
本文介绍的Angew. Chem. Int. Ed.内封面论文作者来自德国、中国、巴西和新加坡四国,他们致力于构建青蒿素和(异)喹啉杂合分子,评估其抗击多重耐药疟疾的活性,并通过蛋白组学鉴定其潜在靶点。

他们按合成双核连接子的化学反应方式,将杂合分子合成设计分为两种方案:(1)铜(I)催化点击反应,(2)酯化、形成酰胺键、原位形成的三级酰胺分子内重排生成二级酰胺。他们共合成17个新杂合分子(图3)。
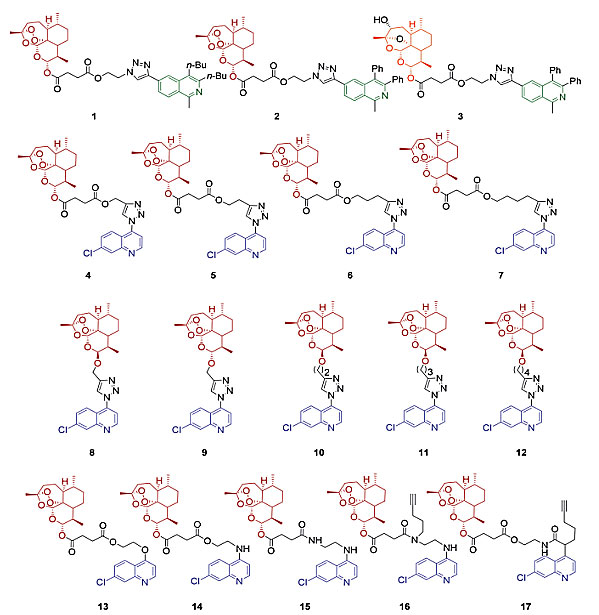
图3. 本文中合成的青蒿素—(异)喹啉杂合分子1-17。图片来源:Angew. Chem. Int. Ed.
在铜(I)催化点击反应中,他们设计的连接基团是生物活性多样的三唑结构,五元三唑环通过1,3-偶极环加成反应合成,是应用极为广泛的连接模块。在方案A中,异喹啉衍生炔(化合物20、21)通过与青蒿琥酯基叠氮化物(22)的点击反应——铜催化的端炔与叠氮的环加成反应(CuAAC)合成青蒿素-异喹啉杂合分子1-3(图4A)。在方案B中,4-叠氮-7-氯喹啉(27)和青蒿琥酯衍生物(23-26)以及二氢青蒿素衍生物(28-32),通过1,3-偶极环化生成青蒿素-喹啉杂合分子4-12(图4B)。在方案C中,青蒿琥酯35与相应的7-氯喹啉衍生物前体(33、34、36、37)反应合成杂合分子13-16,其中35与一级醇34和33的酯化反应分别得到杂合分子13和14,与胺类36和37的酰胺偶联反应分别得到15和16(图4C)。自此,他们得到了16个杂合分子,其中化合物16含炔烃基团。由于蛋白组学鉴定化合物靶蛋白需要炔烃标记分子,化合物16符合要求,还需另一个标记分子,而抗疟活性部分研究表明杂合分子14的活性很好,所以在方案D中,他们对14进行进一步修饰,通过原位形成的三级酰胺的分子内重排得到带炔烃的二级酰胺杂合分子17(图4D)。
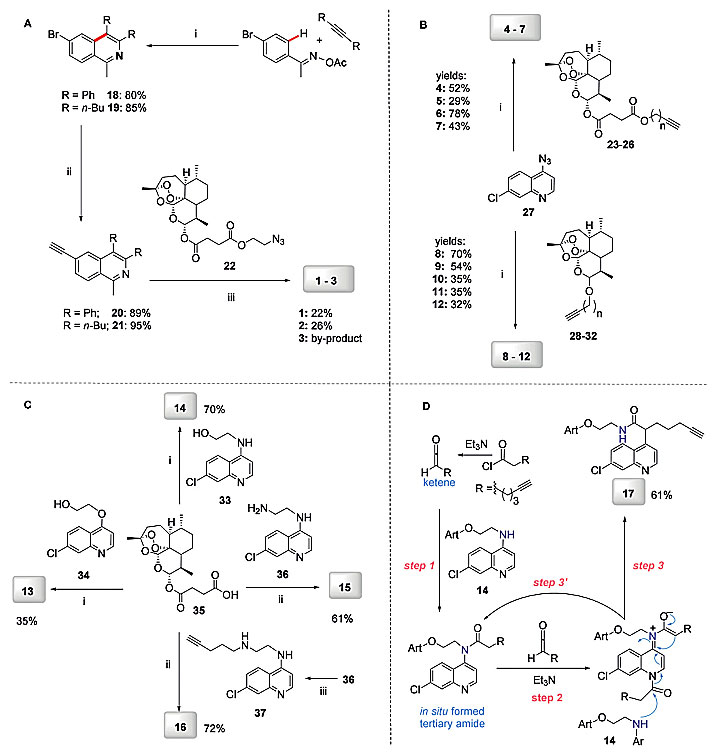
图4. 杂合分子1-17的合成。图片来源:Angew. Chem. Int. Ed.
在体外抗疟活性实验中,研究团队选择耐药疟原虫Dd2和K1、药物敏感疟原虫3D7进行测试。合成的“双核”青蒿素-(异)喹啉杂合分子相对于“单核”分子,展示了更强的抗疟活性,尤其是针对耐药疟原虫,其EC50值(半数有效浓度)从纳摩(nM)量级变为皮摩(pM)量级。研究发现连接基团的类型、杂合物的立体化学结构会显著影响化合物的抗疟活性,连接基团的碳链长度则没有明显影响。其中,杂合分子12、14、15、16对Dd2、K1和3D7都有极高抑制活性,化合物15对K1的EC50值甚至达到780 pM。
在体内抗疟活性实验中,他们构建小鼠恶性疟疾模型。结果显示,化合物14相比于青蒿琥酯和化合物12对小鼠的治愈率更高。在化合物14皮下给药有效的基础上,他们对感染小鼠进行了口服给药实验。结果显示相比青蒿琥酯,化合物14依然有显著治愈效力。事实上,青蒿琥酯只能皮下注射,没有口服效用,且青蒿素、青蒿琥酯抗疟作用迅速,半衰期短。化合物14口服抗疟有效,药效作用持久,能有效延缓疟原虫复发(表1)。
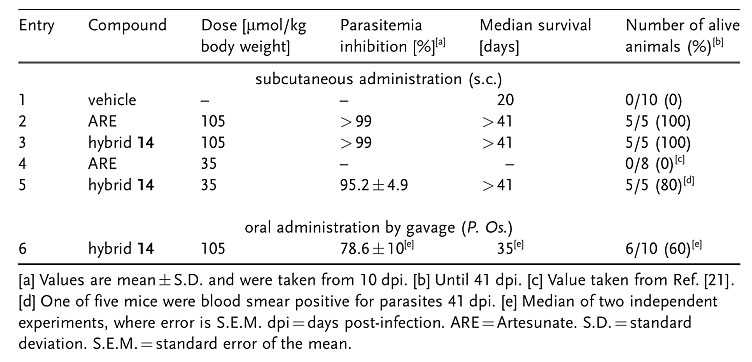
表1. 化合物14和青蒿琥酯抗血液期恶性疟感染小鼠的药理作用。图片来源:Angew. Chem. Int. Ed.
鉴于杂合分子14显著的抗疟活性,研究团队评估其治疗潜力。结果显示,化合物14对感染恶性疟小鼠的治愈率3倍于青蒿琥酯。为进一步探索化合物14抗疟活性的潜在机制,研究团队构建恶性疟感染小鼠模型,分析14在抑制疟色素(hemozoin)形成方面的效力。有趣的是,青蒿琥酯能降低疟原虫数量,却不能抑制疟色素的形成,喹啉能抑制疟色素形成,却不能降低疟原虫数量。只有结构上“双核”的化合物14既能降低疟原虫数量,又能抑制疟色素形成,且两种效力都分别强于青蒿琥酯和喹啉(图5)。
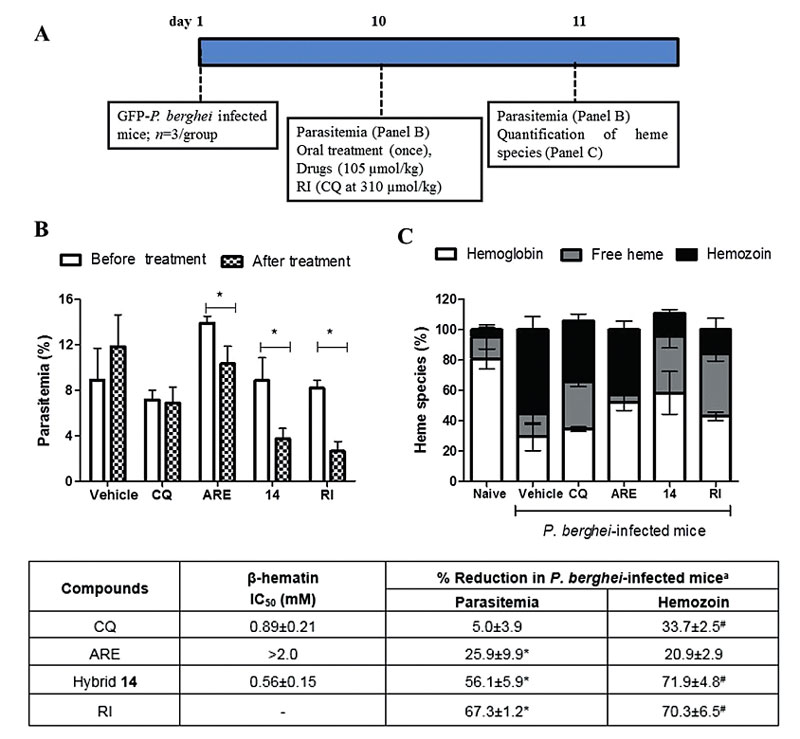
图5. 化合物14、青蒿琥酯、喹啉治疗恶性疟感染小鼠抑制疟原虫、疟色素和血红素的结果。图片来源:Angew. Chem. Int. Ed.
最后,研究团队还利用炔基标记的杂合分子16,、17进行蛋白组学分析,发现了HSP70、rhoptry2、40s核糖核蛋白S15等一系列作用靶标。
面对来势汹汹的耐药性疟疾,现有一线药物青蒿素、(异)喹啉无论是“单刀赴会”的单一疗法,还是“携手并肩”的组合疗法,都日渐倾颓。然而两者“双剑合璧”优化结构得到的杂合分子则可能为抗疟药开发事业开辟新的天地。这一神奇“双核”药物组合,使笔者脑洞大开,联想到国际足坛曾经的传奇“双核”——罗本和里贝里的“罗贝里”组合。笔者希望青蒿素-(异)喹啉两大明星药物的完美结合,也会像足坛的“罗贝里”一样在抗疟药物中光芒万丈。

曾经叱咤足坛的双核“罗贝里”。图片来源于网络
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Artemisinin–(Iso)quinoline Hybrids by C–H Activation and Click Chemistry: Combating Multidrug-Resistant Malaria
Aysun Çapcı, Mélanie M. Lorion, Hui Wang, Nina Simon, Maria Leidenberger, Mariana C. Borges Silva, Diogo R. M. Moreira, Yongping Zhu, Yuqing Meng, Jia Yun Chen, Yew Mun Lee, Oliver Friedrich, Barbara Kappes, Jigang Wang,* Lutz Ackermann,* Svetlana B. Tsogoeva*
Angew. Chem. Int. Ed., 2019, 58, 13066–13079, DOI: 10.1002/anie.201907224
(本文由水村山郭供稿)
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!


























 京公网安备 11010802027423号
京公网安备 11010802027423号