UCLA顾臻团队Matter:构建抗癌脂肪细胞
近日,加州大学洛杉矶分校(UCLA)的顾臻教授(点击查看介绍)团队在Cell 子刊Matter 上发表论文,他们利用脂肪细胞来递送抗癌药物,提出了利用肿瘤微环境中脂肪酸代谢途径促进药物递送的新思路。该团队在动物模型上验证,共轭亚油酸(rumenic acid)可改造脂肪细胞,使其招募机体免疫系统攻击肿瘤细胞,并与基于脂肪酸代谢途径设计的一种新型阿霉素(doxorubicin)前药联用,显著抑制肿瘤生长及术后肿瘤复发。这一研究较为系统地论证了脂肪细胞在抗癌细胞疗法上的应用,有望建立肿瘤以及其他脂代谢相关疾病的新型治疗技术平台。

载药脂肪细胞示意图。图片来源:Matter
肿瘤在增殖的过程中,可招募机体多种细胞共同参与促进肿瘤细胞生长和转移,并抑制机体免疫系统的攻击。其中脂肪细胞可释放游离脂肪酸为肿瘤生长提供能量,同时,肿瘤周围脂肪组织可以释放激素、炎症因子等协同促进肿瘤的炎症环境。研究表明,肿瘤周围脂肪组织可招募巨噬细胞浸润肿瘤组织,并抑制效应T细胞等免疫细胞对肿瘤的攻击,进而在肿瘤的增殖、转移等过程中扮演“帮凶”的角色。另外,脂质分子代谢通路是肿瘤对抗化疗药物的耐药机制之一。因此,靶向肿瘤周围脂肪细胞以及脂质代谢通路成为了近年来药物设计的新思路。
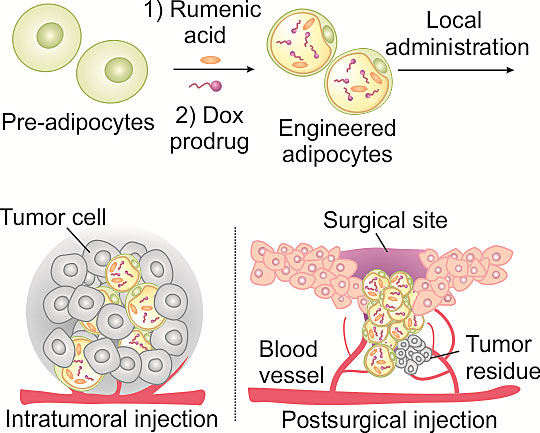
载药脂肪细胞可通过局部注射作用于肿瘤组织或术后创面中。图片来源:Matter
在这项工作中,研究团队首次将脂质分子代谢通路用于抗癌药物递送,并用共轭亚油酸改造脂肪细胞。改造后的脂肪细胞能抑制肿瘤生长,并招募机体免疫细胞杀伤肿瘤细胞。与此同时,研究人员设计了响应肿瘤微环境中活性氧(reactive oxygen species, ROS)的阿霉素前药。通过和油酸分子连接,这种前药分子与脂肪细胞的相容性得到了显著提高,并能在肿瘤细胞里高活性氧的环境中转变为阿霉素,从而提高对肿瘤细胞的选择性杀伤效果。另外,共轭亚油酸能够显著提高这种前药分子在脂肪细胞中的载药量。“改造后的脂肪细胞就像‘特洛伊木马’,能够利用癌细胞本身的代谢途径,实现对癌细胞较为特异性的杀伤。”本文第一作者、顾臻教授团队温迪博士介绍道。
研究团队通过计算机模拟以及实验证明了利用脂肪酸代谢途径递药的可行性,该前药分子可以与脂肪酸结合蛋白4(fatty acid binding protein 4)结合,通过癌细胞的脂肪酸转运途径递送到癌细胞内,从而提高了药物的转运效率和毒性。更重要的是,肿瘤细胞诱发的脂滴分解过程显著促进了脂肪细胞中的药物释放,加强了药物对肿瘤细胞的杀伤效果。
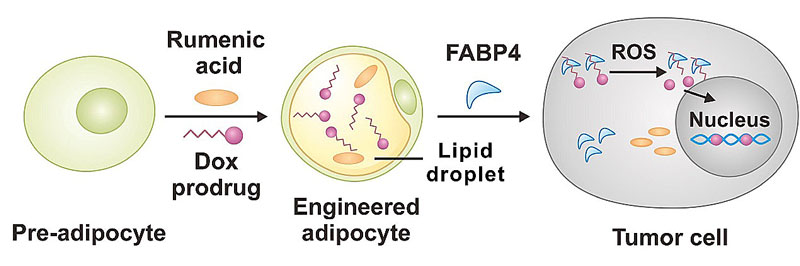
共轭亚油酸与阿霉素前药的装载及作用示意图。图片来源:Matter
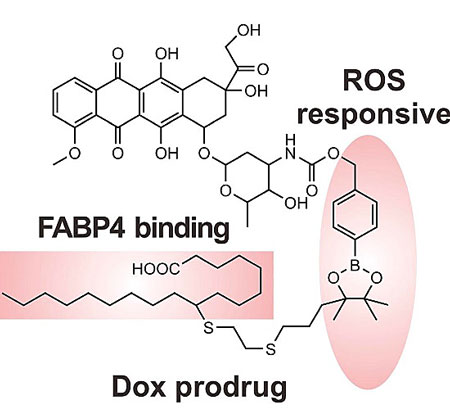
阿霉素前药的化学结构示意图。图片来源:Matter
值得一提的是,这种利用肿瘤微环境细胞作为药物载体的递药方式,有望为细胞疗法开辟新的思路。而利用代谢途径递药的方式,可提高药物在肿瘤组织中的吸收,为肿瘤以及其他与脂代谢相关的疾病的药物设计提供新的方向。顾臻教授介绍道:“团队正在尝试利用类似的方法运送其它抗肿瘤药物,并同时验证这种药物设计策略的其他应用。”
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Adipocytes as Anticancer Drug Delivery Depot
Di Wen, Jinqiang Wang, George Van Den Driessche, Qian Chen, Yuqi Zhang, Guojun Chen, Hongjun Li, Jennifer Soto, Ming Liu, Masao Ohashi, Zejun Wang, Peter Abdou, Quanyin Hu, Gianpietro Dotti, Song Li, Denis Fourches, Zhen Gu
Matter, 2019, DOI: 10.1016/j.matt.2019.08.007
导师介绍
顾臻
https://www.x-mol.com/university/faculty/26755
(本稿件来自Matter)
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!




























 京公网安备 11010802027423号
京公网安备 11010802027423号