我们距离自动化从头药物设计还有多远?
提到新药研发,大家不免都有这种印象:投资高、时间长、风险大。虽然药物设计和筛选技术一直在进步,但疾病是复杂的,即使研发的药物过五关斩六将成功上市,但还要面临不良反应、市场销售、国家政策等诸多未知因素的考验。其实要解决这些问题也不是没有办法,那就是多设计几个足够优秀的候选药物。
药物化学领域的读者估计这会儿心里一定在不屑地说,“你说的容易”!的确,发现一个能上临床试验的药物,就已经要感谢运气爆棚了(点击阅读:药物化学家一生发现新药的几率有多大?),遑论好几个好用又好卖的“重磅新药”?
不过,随着X-射线衍射、NMR、电子显微镜等技术的快速发展,靶蛋白的结构参数逐渐明晰。另一方面,计算性能的大幅提升和硬件价格的降低,使得计算机辅助药物设计工具成为科学家不可或缺的帮手。现在各种计算机算法已经可以进行虚拟筛选或直接给出新分子结构,并帮助科学家优化苗头化合物的成药性及理化性质。那么现在计算机能不能如AlphaGo那种人工智能那样,给它一个化学结构自动从头设计药物分子呢?现在药物研发圈里的人工智能、机器学习等热门话题又进展如何?
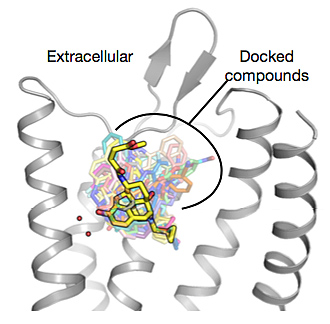
基于结构的药物虚拟筛选。图片来源于网络
在药物设计领域,计算机程序在上世纪已经辅助研究人员开发了一些药物。最常见的方法是以某个已知结构的蛋白为靶点利用分子对接等虚拟筛选技术在海量化学结构中找到那个苗头化合物(hit compound)。除此之外,还有一些基于小分子化学结构的药物设计程序,比如从头药物设计(de novo design)程序。近期,苏黎世联邦理工学院(ETH Zürich)的Gisbert Schneider博士(点击查看介绍)等人总结近几年自动从头药物设计的文献并详细列举了10个药物靶标案例以便读者能够纵览全局或者了解前沿方向。相关论文发表在Angew. Chem. Int. Ed. 杂志上。

Gisbert Schneider博士。图片来源:ETH Zürich
1. β分泌酶抑制剂
BACE-1是神经退行性疾病的靶标之一,但成药性颇具挑战。Fishwick等报道了基于蛋白结构的从头药物设计程序SPROUT,设计了非多肽结构的ß分泌酶BACE-1抑制剂(J. Med. Chem., 2013, 56, 1843)。通过BACE-1和类多肽配体的复合物X-射线结构,SPROUT解析了关键活性位点,并设计了最初的化合物1。合成化合物1后并测试它的生物活性,发现它的活性较弱(IC50 = 323 μM)。结构优化后得到化合物2,它的活性中等(IC50 = 27 μM)。这个案例证实了基于自动结构设计得到可合成化合物作用于靶标的可行性。
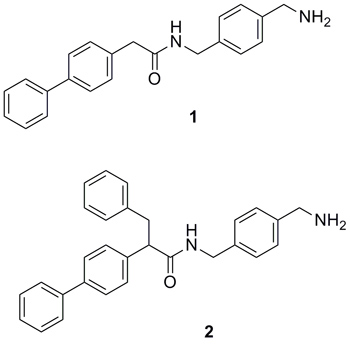
图片来源:Angew. Chem. Int. Ed.
2. Aurora A激酶A抑制剂
VX-680是 pan-Aurora激酶抑制剂,具有很高的抗Aurora活性(Ki = 0.6 nM),在临床试验中,因QT间期延长的心脏问题而被终止。Rodrigues等通过基于配体的从头药物设计程序DOGS(Design Of Genuine Structures),希望设计一个全新的化学骨架(Chem. Sci., 2013, 4, 1229),具有和VX-680相似的活性,但避免诱发心脏问题,同时突破围绕这一结构的知识产权限制。DOGS程序基于88个骨架,产生了172个化学结构。因芳香磺酰胺结构片段在打分系统中得高分的情况较多,而且化学合成可行性较高,相应的化合物3和4被筛选出来进行合成。DOGS另一个优势是它可以设计合成路线,设计算法来源于化学转化规则。体外实验发现,100 μM的3仅能抑制5%的Aurora A。4的活性为IC50 = 10 μM,适合从苗头化合物到先导化合物的优化。3和4活性的巨大差异很可能来自咪唑结构片段。在此指导下,他们通过优化得到了化合物5(IC50 = 2.7 μM)。
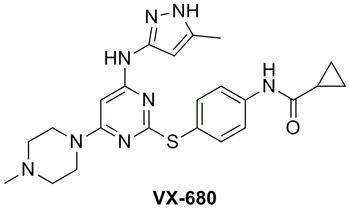
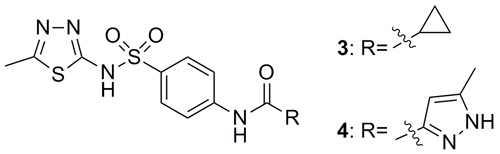
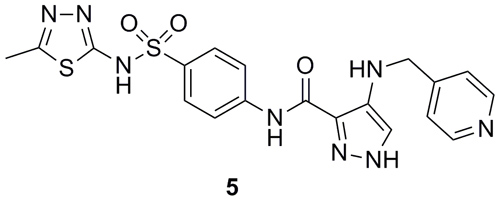
图片来源:Angew. Chem. Int. Ed.
从这个案例中可以看到以下三点:(1)化合物5的结构已经于初始的VX-680截然不同,是全新的结构。(2)该程序仅需要一个抑制剂的结构就可以启动程序,甚至蛋白质结构都不需要,因此这套方法具有广泛的应用范围。(3)设计的化合物能够大多可以被合成出来并用于测试活性。
从Aurora A和抑制剂的复合物晶体结构开始,Park等用片段数据库中用基于结构的虚拟筛选找到了一个关键片段结构MPPA,他们的秘诀是自动对接,并且修改了打分功能(J. Chem. Inf. Model., 2018, 58, 700)。以铰链-结合部位为起始点,团队用LigBuilder聚焦于Aurora A的片段结构数据库利用从头药物设计手段设计新化合物,遵循药物设计中的类药5规则,最终挑选了35个化合物,合成了17个,活性最好的化合物为6(IC50 = 0.012 nM)。

图片来源:Angew. Chem. Int. Ed.
3. COX-2和LTA4H双重抑制剂
多重药理学近年来也得到关注,即一个化合物通过作用于1个以上的靶标达到治疗效果。Shang等使用从头药物设计程序LigBuilder设计作用于环氧化酶-2(COX-2)/5-脂质氧化酶(5-LOX)/白三烯A4水解酶(LTA4H)的化合物,以达到更好的抗炎症效果(J. Chem. Inf. Model., 2014, 54, 1235)。作者从这三个靶标已知抑制剂中提取片段结构,得到了21个化合物,然后在高浓度下(1 mM)进行活性测试得到9个苗头化合物。LigBuilder 程序对这些结构片段进行多种结合模式的计算,设计了110万个化合物,从中筛选出前1000个继续研究,最终合成了6个化合物,其中化合物7的活性最好,100 μM浓度下对COX-1和COX-2的抑制率为90%,LTA4H的抑制率为43%,从而进入第二轮从头药物设计,得到化合物8,第三轮得到化合物9。相比于COX1,化合物9对COX2有很好的选择性(约11倍)。
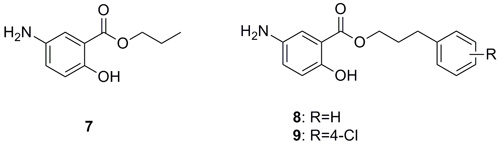
图片来源:Angew. Chem. Int. Ed.
4. 幽门螺杆菌HtrA抑制剂
幽门螺杆菌(Helicobacter pylori)可导致胃/十二指肠溃疡甚至胃癌。丝氨酸蛋白酶致病因子HtrA(high temperature reguirement A)是幽门螺杆菌和其他致病菌的靶标,现在可用的化合物是罗丹宁衍生物10,但它存在活性弱、溶解度差、以及罗丹宁骨架自身的问题。
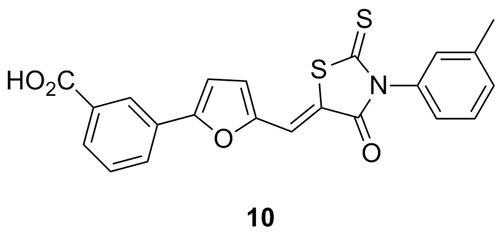
图片来源:Angew. Chem. Int. Ed.
Perna等人采用DOGS软件以10为起点(Angew. Chem. Int. Ed., 2015, 54, 10244),设计了1707个化合物,通过溶解度结合三维结构进行筛选,选取了其中的65个化合物进行合成,化合物11最符合以下4项要求:溶解度和切合度排名靠前;没有Michael加成受体结构;与化合物10的结构区别很大;全新的化学结构类型。
经两步反应可合成11,它的亲和力和化合物10类似(KD = 37μM),但配体效率LE(ligand efficiency)更好。构型关系研究中,它的类似物12的活性最好(KD = 37 μM,LE = 0.3),并且都有体外抗幽门螺杆菌活性。
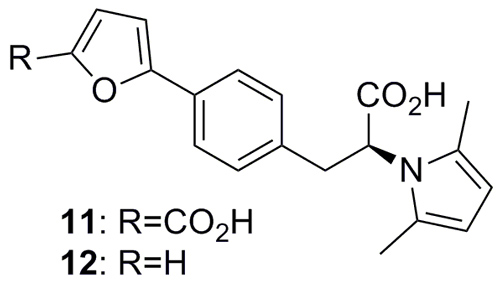
图片来源:Angew. Chem. Int. Ed.
5. DAPK3抑制剂片段类似物
死亡关联蛋白激酶3(DAPK3)是丝氨酸/苏氨酸激酶,可作为治疗高血压和平滑肌疾病的靶标。以法舒地尔Fasudil(IC50 = 1.2 μM)为起点,Schneider等人使用DOGS进行基于配体的从头药物设计(Angew. Chem. Int. Ed., 2015, 54, 15079),构建了521个化合物,其中357个符合类似片段的标准。进一步基于机器学习算法的ChEMBL预测,选取了化合物13,其对DAPK3的抑制浓度为52 μM,但它的配体效率较高(LE = 0.4),在27种激酶中的选择性很好,与法舒地尔的结构相差也很大,但它是已知化合物阿佐塞米Azosemide(IC50 = 2.1 μM)的亚结构,这也从侧面说明从头药物设计策略得到的化合物具有再优化的潜力。

图片来源:Angew. Chem. Int. Ed.
6. 选择性MMP-2抑制剂
基质金属蛋白酶2(MMP-2)和MMP-9类似,要开发选择性的抑制剂并不简单。Adhikari等用Bayesian模型从MMP-2/MMP-9抑制剂中筛选出选择性作用于MMP-2的结构片段(Bioorg. Med. Chem., 2016, 24, 4291),从中组合得到化合物14。化合物14对MMP-2的IC50 为0.9 μM,相比于MMP-9具有8倍的选择性。将14和MMP-2结构对接,用从头药物设计程序LUDI进行基于片段的结构优化,从而得到众多衍生物,其中化合物15对MMP-2的IC50 = 24 nM,选择性提高至21倍。

图片来源:Angew. Chem. Int. Ed.
7. TRPM8 拮抗剂
来自大戟科植物毒叶下珠(Phyllanthus engleri)的天然产物(-)-Englerin A(化合物16)具有抗细胞增殖的作用,可以通过选择性激活瞬时受体电位钙离子通道(transient receptor potential canonical 4/5 calcium channels)杀死肾癌细胞,但它的急性毒性较大,不适合作为药物。Friedrich等人用DOGS软件以Englerin A为模板进行设计(Angew. Chem. Int. Ed., 2016, 55, 6789),然后用CATS近似度打分,选出化合物17和18,尽管结构仍然复杂,但可以化学合成,进一步简化为化合物19和20。它们对TRPM8亚型的活性较好(KB = 1.4 μM和0.2 μM),但高浓度10 μM下不会抑制TRPV1钙离子通道,而且不具有细胞毒性。药效学研究发现,化合物20的S构型活性更好,呋喃环可以进行结构衍生,后续得到的化合物中,仅有一个能够阻断离子通道,没有化合物的活性高于20,这说明软件可以模拟天然产物进行结构简化得到高活性化合物。
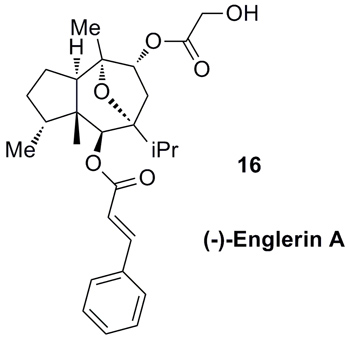
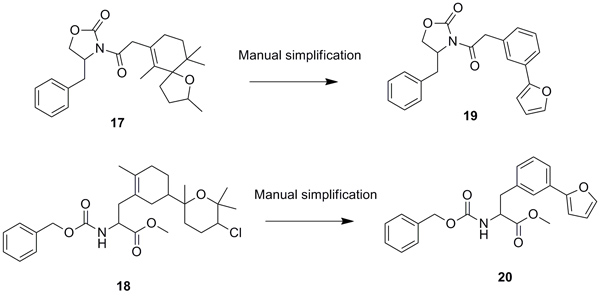
图片来源:Angew. Chem. Int. Ed.
8. β2-肾上腺素能受体拮抗剂
Chevillard用GVM (Growing via merging )流程设计β2-肾上腺素能受体拮抗剂(J. Med. Chem., 2018, 61, 1118)。以5个确定的核心片段开始,SEED程序将核心片段和还原胺化试剂组合得到新结构。再将得到的新结构与β2-肾上腺素能受体再次重新对接,从中选出了8个化合物进行合成,其中化合物21的活性最好,为最初活性片段的40倍,并且保留了很好的配体效率。

图片来源:Angew. Chem. Int. Ed.
9. 维生素A酸 X 和过氧化物酶体增殖物激活受体激动剂
Schneider等用“generative artificial intelligence“设计具有期望生物活性的类药化合物(Mol. Inf., 2018, 37, 1700153)。这套模式通过类神经网路从ChEMBL数据库的生物活性分子中学习化学结构。本案例中利用具有生物活性的25个脂肪酸类似化合物进行微调,作用于两种核受体,视黄醇类X受体(RXRs)和过氧化物酶体增殖物激活受体(PPARs)。以常见于激动剂的羧酸为特殊片段,类神经网络生成了1000个结构全新的候选化合物,与25个训练化合物位于相同的化学空间,经过筛选最终选取了5个化合物进行合成。生物活性测试结果如下表所示,化合物活性大多在纳摩尔和微摩尔数量级上,符合苗头化合物的活性要求。这里注意的是,该程序设计出的化合物是可以合成的,而这正是以往从头药物设计程序的弱项。
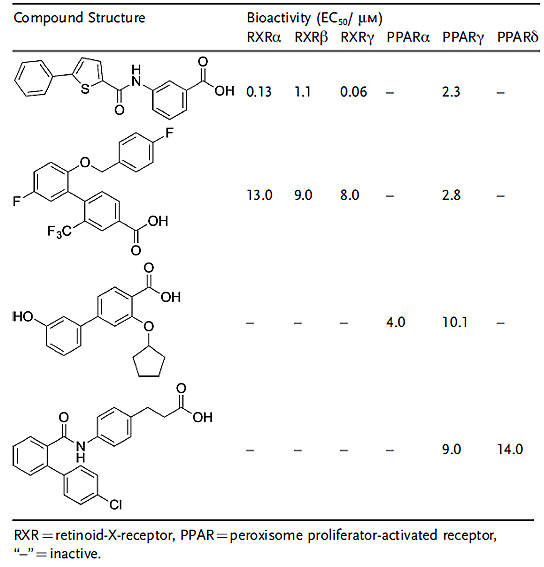
人工智能策略设计的化合物结构及生物活性。图片来源:Angew. Chem. Int. Ed.
随后,这个课题组还成功运用这个工具开发了基于天然产物缬草酸valerenic acid的PXR配体,得到化合物22,它能在低微摩尔浓度下激活所有的三个RXR亚基,发挥RXRβ的高转录激活效率。

图片来源:Angew. Chem. Int. Ed.
10. JAK3抑制剂
In Silico Medicine的一个科研小组应用新型的人工智能程序 “entangled conditional adversarial autoencoder (ECAAE)”设计了新颖的JAK3抑制剂(Mol. Pharm., 2018, 15, 4398)。他们从 ChEMBL数据库中筛选出作用于JAK3和JAK2的化合物,以望设计出只作用于JAK3 的分子。程序初始设计了30万个结构,通过分子对接和理化性质计算,筛选出5000个结构,然后进行分子动力学计算,最后药物化学家选出100个分子。其中化合物23被合成出来,体外测试发现它对JAK3的IC50 = 7 μM,分子量仅有318,而且对JAK2表现出一定的选择性(IC50 = 18 μM)。
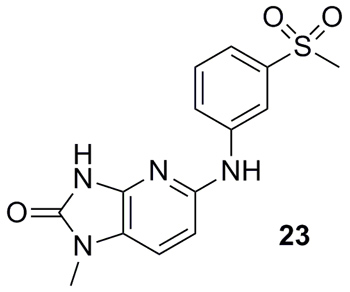
图片来源:Angew. Chem. Int. Ed.
基于以上案例,Gisbert Schneider博士等人对当前自动从头药物设计进行了如下总结:
1)目前的程序算法,可以设计出可合成的化合物,并且能够得到期望的高生物活性,这些化合物可以作为从苗头到先导化合物的起点。
2)目前从头药物设计流程还需要人工输入,包括分子对接和程序筛选。另一方面,化合物设计需要人工干预,使化合物更容易合成。
3)从头药物设计基于配体的虚拟筛选,即使仅仅知道一个已知配体结构,也可以将从头药物设计程序扩展到其他项目。很多案例证实了新设计的化合物结构和起点截然不同。
不断出现的人工智能也影响着药物化学家,那么以后的自动从头药物设计会向哪方面发展呢?Gisbert Schneider博士等人作了如下预测:
1)设计结构程序可以立刻启用,并且实时进行分子模拟,用户与AI互动增强。
2)设计的绝大多数分子结构是可合成的,额外的AI负责逆合成分析,设计合成路线。
3)可以在线从最新的活性数据中学习,并且始终自动优化预测精确度。
4)在分子设计的循环中,学习功能激活,能够在合成结构和测试上给出最优的建议。
如今,人工智能已经渗入到科技和生活的各个领域,深度参与药物设计也是大势所趋。科技的进步和人类的期望密不可分。那么,你理想中的人工智能药物发现是什么样子呢?评论区里见!
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Automated De Novo Drug Design: Are We Nearly There Yet?
Gisbert Schneider, David E. Clark
Angew. Chem. Int. Ed., 2019, 58, 10792-10803, DOI: 10.1002/anie.201814681
导师介绍
Gisbert Schneider
https://www.x-mol.com/university/faculty/2777
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!


























 京公网安备 11010802027423号
京公网安备 11010802027423号