Principinol D的汇聚式全合成
Grayanane二萜类化合物是结构新颖的碳酸酐酶和磷酸酶的变构抑制剂。这些分子靶标的各种亚型结构在天然产物及生物活性分子中广泛存在。Grayananes属于广义的重排型贝壳杉烷(kaurane)类分子,该类分子还包括赤霉素烷和6,7-seco-kaurane(图1A)。将贝壳杉烷6,6-A/B环重排为5,7-环可形成四环二萜分子grayanane。1962年,Irland等人完成了(±)-kaurene的首例全合成。随后,许多课题组利用不同的合成策略完成了该类天然产物的全合成。然而,大部分已分离得到的kaurane二萜类化合物通过以往报道的合成方法仍然无法制备。
基于这些化合物立体化学的复杂性,化学家们曾采用线性环化策略对其进行构建。而如果可以设计一种按照立体中心将分子分为两个主要片段的汇聚式合成策略,将会为合成grayanane类天然产物提供一条高效实用的途径。近日,美国耶鲁大学化学系的Timothy R. Newhouse(点击查看介绍)课题组就利用汇聚式的合成策略,完成了grayanane principinol D(1)的首例全合成。其中中心七元环在合成后期构建,双环[3.2.1]辛烷片段通过Ni催化的α-乙烯基化反应构建。相关工作发表在J. Am. Chem. Soc.上。

图1. 目标分子结构及其逆合成分析。图片来源:J. Am. Chem. Soc.
与其他grayanane二萜化合物类似,principinols具有高度氧化的四环骨架,其中包括双环[3.2.1]辛烷结构。Principinol D(1)靠近最左边的五元环具有三个手性中心,它们在空间上与另外五个处于双环[3.2.1]辛烷体系的手性中心分开。为了实现多种相关类似物的合成,作者设计了一种汇聚式的策略,两个子片段将在合成后期进行连接,构建核心骨架并同时合并两组手性中心。这种拓扑简化策略与以往合成grayanane类分子的工作明显不同。
作者计划利用两组C-C键形成反应来合并这些片段:环戊烯基片段(4)和双环[3.2.1]辛烷片段(3)之间的1,2-加成反应以及随后SmI2介导的还原环化。镍催化的α-乙烯基化反应可实现双环片段的裂解,环己酮邻位双官能化可得到相应的六元环。化合物4则很容易从已知化合物5通过1,3-二噻烷的加成、MOM保护和二噻烷脱保护得到,三步总收率为55%。
作者在DMPU和催化量CuBr•SMe2的存在下,从环己烯酮与乙烯基溴化镁的1,4-加成出发合成双环[3.2.1]辛烷片段3,然后用Mander试剂捕获得到β-酮酯7,7与2,3-二溴丙烯进行烯丙基化。作者希望在酮的存在下可以选择性还原酯,以减少不必要的氧化还原操作。金属酰胺或膦的亲核加成原位保护酮的常规方案并不可行。同样地,将酮转化为烯醇化物(使用LiHMDS、KHMDS、NaHMDS或LDA作为碱)进行掩蔽并用还原剂(LiAlH4、DIBAL-H、AlH3、LiBH4或LiEt3BH等)处理可导致底物分解。最终作者通过弱碱性的Zn(TMP)2对酮去质子化形成烯醇化物,再用市售的LiBH3NMe2进行还原可形成酮醇8。TBS保护伯醇得到乙烯基化前体9,为单一非对映异构体,三步总产率为35%。
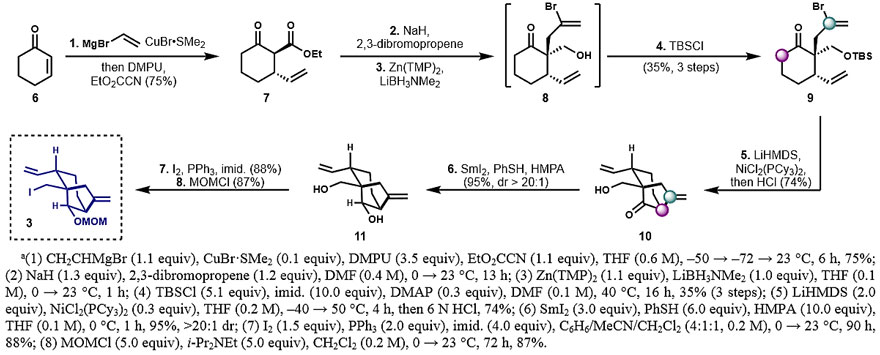
图2. 片段3的合成。图片来源:J. Am. Chem. Soc.
为了从卤化物9构建双环10,作者考察了各种α-乙烯基化底物和多种反应条件,最终使用NiCl2(PCy3)2作为预催化剂、LiHMDS作为碱进行乙烯基化,比Pd催化的条件下进行反应效果更好。保护的酮-醇消除TBS保护基后需要对酮10进行非对映选择性还原。氢化硼或铝化合物(NaBH4、Et2BOMe/NaBH4、NaBH4/CeCl3、DIBAL、Al(O-i-Pr)3)参与还原反应主要产生非预期的非对映体。而在H2O存在下使用SmI2介导还原反应,目标产物仍然不是主要的(d.r. = 1:2)。使用HMPA和氢原子给体PhSH参与反应可以得到预期的产物(95%,>20:1 d.r.),可能是因为HMPA提高了钐配合物的还原电位。作者以C6H6/MeCN/CH2Cl2作为三相溶剂体系,在4:1:1的条件下,将伯醇转化为碘化物,再对二级醇进行MOM保护得到了偶联所需的双环化合物3。
为了连接这两个片段,作者用叔丁基锂处理外消旋的双环[3.2.1]辛烷中间体3,然后添加环戊醛4(er = 93:7),以5:5:1:1的d.r.值得到可分离的非对映体混合物,总收率为62%,最终以26%的收率得到预期的单一非对映体。他们进一步使用MOMCl对二级醇保护得到化合物12,由于该手性中心存在空间位阻,很难引入TBS和TES等其他保护基团。烯丙基硅醚经脱保护和氧化转化为烯酮,在1,1-二取代烯烃的存在下,选择性氧化裂解单取代烯烃得到烯酮-醛13。DABCO作为一种关键的添加剂对产物的预期选择性具有重要影响,而NMO、2,6-lutidine、甲磺酰胺等其他方法的效果都较差。
作者还尝试使用SmI2介导的方法构建七元环。经过系统的优化,他发现在水的存在下使用SmI2处理烯酮-醛13,能以单一对映体、63%的收率得到所需的四环化合物2。NOESY NMR分析测定了该化合物的结构和立体化学,X射线晶体衍射可确定该化合物的绝对构型。
构建碳环核心结构2后还面临着很大的挑战:在C3处引入二级醇羟基,在C10处引入烯基,在C16处引入叔醇羟基。作者发现用吡啶作为缓冲剂的Dess-Martin试剂氧化2可以得到中间体14。在五元环酮存在的情况下,他们尝试了对七元环上的酮羰基进行选择性烯化。其他烯化条件(例如Wittig、Tebbe、Petasis、Nysted等)无法形成所需的环外烯烃。但是,使用Me3SiCH2Li参与反应可有效得到Peterson加合物15。
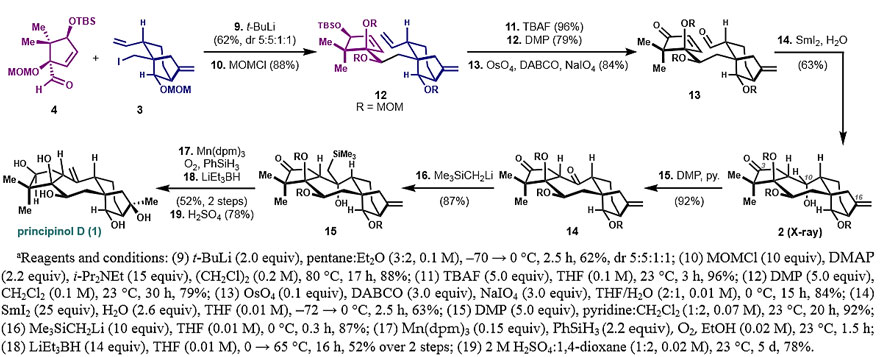
图3. principinol D的全合成。图片来源:J. Am. Chem. Soc.
随后,环外烯烃在Mn(dpm)3、PhSiH3和O2存在下发生Mukaiyama水化反应,C16位引入叔醇羟基。在大多数情况下,环戊酮15在C3处还原时主要产生非预期的α-醇,而与LiEt3BH反应则可在C3处引入所需的醇羟基。体系加热后Peterson加合物发生消除,并在C10处引入亚甲基,产物为单一的非对映体,两步产率52%。H2SO4消除MOM保护基的效果良好,以78%的产率得到了principinol D。
总结
Timothy R. Newhouse课题组以19步汇聚式的策略完成了principinol D的首次全合成,该工作的关键步骤为汇聚式片段的偶联、SmI2介导的还原环化、Ni催化的α-乙烯基化形成双环[3.2.1]辛烷骨架以及SmI2介导双环酮的非对映选择性还原。这种合成策略对于grayananes家族天然产物的多样性全合成及系统的生物活性研究都具有重要的意义。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Convergent Total Synthesis of Principinol D, a Rearranged Kaurane Diterpenoid
Aneta Turlik, Yifeng Chen, Anthony C. Scruse, Timothy R. Newhouse
J. Am. Chem. Soc., 2019, 141, 8088-8092, DOI: 10.1021/jacs.9b03751
导师介绍
Timothy R. Newhouse
https://www.x-mol.com/university/faculty/1301
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!



























 京公网安备 11010802027423号
京公网安备 11010802027423号