清华大学林金明团队:DNA探针用于检测流体剪切力促进肿瘤细胞和细菌的粘附
近年来研究发现肿瘤与微生物之间存在深入联系,除了免疫相互作用外,哺乳动物细胞和细菌之间还存在其他各种相互作用,如肠道微生物会诱导乳腺癌的发生。因此研究癌症细胞和细菌之间的相互作用对于肿瘤的发生与治疗具有重要意义。其中,肿瘤细胞对细菌识别的机械传感机制在炎症和吞噬作用中起重要作用。但是目前在流体剪切力下实现生物分子在质膜中的精确亚细胞定位的研究仍然较为局限。

图1. 在微通道中流体剪切力增强肿瘤细胞的细菌受体聚集
近期,清华大学的林金明(点击查看介绍)团队开发了基于DNA探针的生物分子可视化系统,实现实时观察在流体剪切力下,肿瘤细胞与细菌相互作用期间宿主细胞膜上增强的受体聚集现象(图1)。为了在肿瘤细胞与细菌相互作用期间监测膜蛋白、细胞表面糖类和脂质双层的行为和功能,使用了三种不同的标记策略分别用荧光探针标记这三种组分(图2)。同时将微流控芯片用于癌细胞培养和处理,实现精确的流量控制和实时荧光观察。研究发现,当MCF-7细胞暴露于大肠杆菌溶液产生的剪切应力时,宿主细胞膜蛋白会聚集并发出强烈的荧光(图3),但是糖类和磷脂没有聚集。结果表明膜蛋白,细胞表面糖类和磷脂双层在识别过程中以不同方式起作用。该研究不仅揭示了新的细胞-细菌机械传导机制,而且还提供了一种能够原位和动态指示细胞对机械刺激的反应的通用方法。
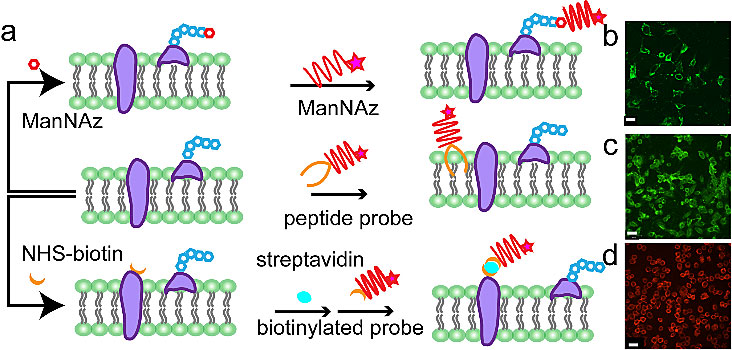
图2. 三种细胞膜组分的不同标记策略

图3. 流体剪切力下大肠杆菌引起MCF-7细胞膜蛋白聚集
这一成果近期发表在Analytical Chemistry 上,第一作者为清华大学化学系博士生张婉玲同学。上述研究得到国家自然科学基金的资助。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

In Situ Monitoring of Fluid Shear Stress Enhanced Adherence of Bacteria to Cancer Cells on Microfluidic Chip
Wanling Zhang, Sifeng Mao, Ziyi He, Zengnan Wu, Jin-Ming Lin*
Anal. Chem., 2019, 91, 5973–5979, DOI: 10.1021/acs.analchem.9b00394
导师介绍
林金明
https://www.x-mol.com/groups/Linlab
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!



























 京公网安备 11010802027423号
京公网安备 11010802027423号