Angew. Chem.:仿病毒融合囊泡原位检测外泌体miRNA
外泌体是由细胞分泌的直径为30~150 nm的细胞外囊泡,内含丰富的蛋白质、脂质、核酸等成分,是细胞间信息传递的重要方式。大量研究发现,外泌体miRNA可作为重要标志物用于疾病的诊断、疗效评估和预后分析。目前外泌体miRNA的检测方法主要是先通过超速离心等方法分离外泌体,提取RNA后再经逆转录-聚合酶链反应检测目标miRNA。然而上述方法存在外泌体损坏、操作繁琐、耗时等问题。此外,在检测过程中容易造成miRNA的降解和损失,从而影响结果的准确性。如何实现外泌体miRNA的简单、快速、准确检测是亟需解决的关键科学问题和重要临床需求。
近日,上海交通大学张川研究员、朱新远教授联合上海交通大学附属第六人民医院南院冯景教授团队,开发了一种仿病毒融合囊泡用于外泌体miRNA的快速、原位检测(图1)。不同于传统方法将外泌体miRNA从囊泡中取出进行检测,新的方法反其道而行之,利用囊泡融合主动将检测探针送入外泌体,从而实现miRNA原位无损荧光检测。在实验设计中,团队成员受自然界中病毒膜与细胞膜融合现象的启发,通过基因工程技术在细胞膜表面表达人副流感病毒的血凝素-神经氨酸酶(hemagglutin-neuraminidase,HN)蛋白和融合(fusion,F)蛋白,通过挤出法制备包载荧光分子信标的仿病毒融合囊泡。囊泡表面的包膜蛋白与外泌体表面的唾液酸受体结合后引起囊泡与外泌体的高效融合,从而将囊泡内的分子信标递送到外泌体内部,分子信标与外泌体内特异miRNA结合后,荧光信号由关闭转为开启状态,从而实现外泌体内miRNA的准确检测。
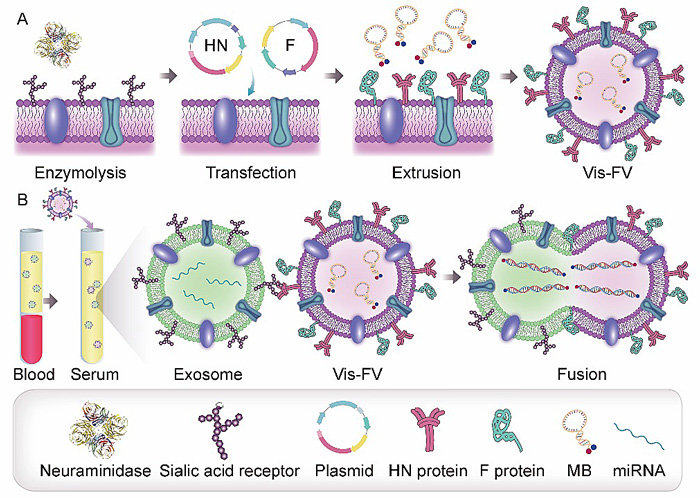
图1. 仿病毒融合囊泡原位检测外泌体内miRNA
研究发现仿病毒囊泡与外泌体共同孵育一定时间后,通过透射电镜可以观察到处于不同融合阶段的中间产物(图2A)。共聚焦显微镜成像显示按不同比例孵育后,仿病毒囊泡(红色)和外泌体(绿色)均发生了一定程度的融合(黄色,图2B)。荧光能量共振转移实验证实不具有病毒包膜蛋白的对照囊泡则几乎不与外泌体融合,而仿病毒囊泡膜可以与外泌体膜在1.0 h内即可实现融合(图2C)。将仿病毒融合囊泡加入到临床肿瘤病人的血清中后,通过流式分析可以发现仿病毒融合囊泡与血浆中细胞外囊泡融合后产生具有不同强度荧光信号的两个群落(图2D&E),说明该仿病毒囊泡可以通过检测外泌体miRNA有效区分肿瘤患者和健康人的血清。
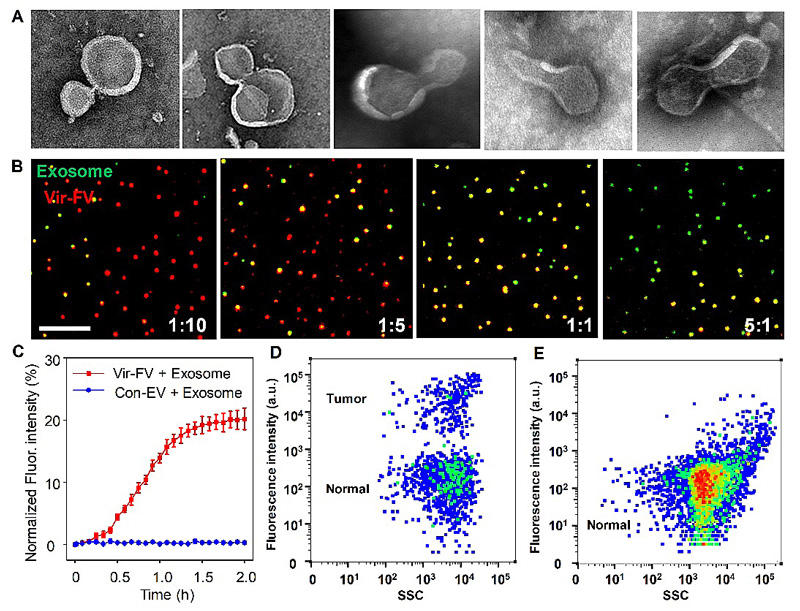
图2.仿病毒囊泡融合外泌体,原位检测外泌体miRNA
仿病毒囊泡检测外泌体miRNA不需要复杂的分离检测步骤,速度快,耗时短。同时,该方法无需破坏外泌体,可避免miRNA的降解,实现了外泌体内miRNA的准确、快速、原位检测,对肿瘤的诊断、疗效评估和预后分析具有重要意义。
此项研究受到国家自然科学基金、上海健康医学院协同创新重点专项等基金的支持,高西辉博士、李莎硕士研究生为共同第一作者,张川研究员和冯景教授为共同通讯作者。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Rapid Detection of Exosomal MicroRNAs Using Virus-Mimicking Fusogenic Vesicles
Xihui Gao, Sha Li, Fei Ding, Hongjia Fan, Leilei Shi, Lijuan Zhu, Jing Li, Jing Feng, Xinyuan Zhu, Chuan Zhang
Angew. Chem. Int. Ed., 2019, DOI: 10.1002/anie.201901997
导师介绍
张川
https://www.x-mol.com/university/faculty/12622
朱新远
https://www.x-mol.com/university/faculty/12602
(本稿件来自Wiley)
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!




























 京公网安备 11010802027423号
京公网安备 11010802027423号