生源合成启发的JACS:(-)-Mitrephorone B的C-H键氧化合成(-)-Mitrephorone A
ent-trachylobane类天然产物mitrephorone A、B、C(1-3)与二萜类 ent-atiserene、ent-beyerene和ent-kaurene在结构上有一定的关联,但前者的氧化模式比较罕见,在合成上也极具挑战性(图1)。初步的生物活性筛选显示,1-3具有中等的抗微生物和抗癌活性。可能的生源合成始于香叶基香叶基焦磷酸酯(GGPP,C20)的环化反应,生成ent-pimarenyl碳正离子4。Tantillo阐明了4转化为ent-trachylobane骨架5的机理(J. Am. Chem. Soc., 2010, 132, 5375–5386),并且排除了先前假定的二级碳正离子的过程,5在酶催化下合成mitrephorone B(2),它是一个关键的中间体,可以选择性地氧化生成1和3。在mitrephorone B(2)的形成过程中,无论是先氧化反式十氢萘骨架,还是先将C19位官能团化,都可以得到ent-trachyloban-19-oic acid(6)。值得注意的是,如果能模拟这种mitrephorone B(2)氧化生成mitrephorone A(1)的生源途径,会减少如扩环、[2+2]-环加成反应和亲核取代反应等常规形成氧杂环丁烷方法的底物局限性。
2018年,Carreira课题组采用极性翻转的策略实现了1的合成(J. Am. Chem. Soc., 2018, 140, 16704–16710)。在此基础上,奥地利因斯布鲁克大学Thomas Magauer 教授课题组首次报道了mitrephorone B(2)的全合成,并通过生源合成启发的后期C-H键铁催化氧化或电化学氧化合成mitrephorone A(1),仅需一步就可以得到高度取代的氧杂环丁烷。同时,在该条件下却没有形成骨架上没有氧杂环丁烷但在C2位上带有酮基的mitrephorone C(3)。相关成果发表在J. Am. Chem. Soc. 期刊上。
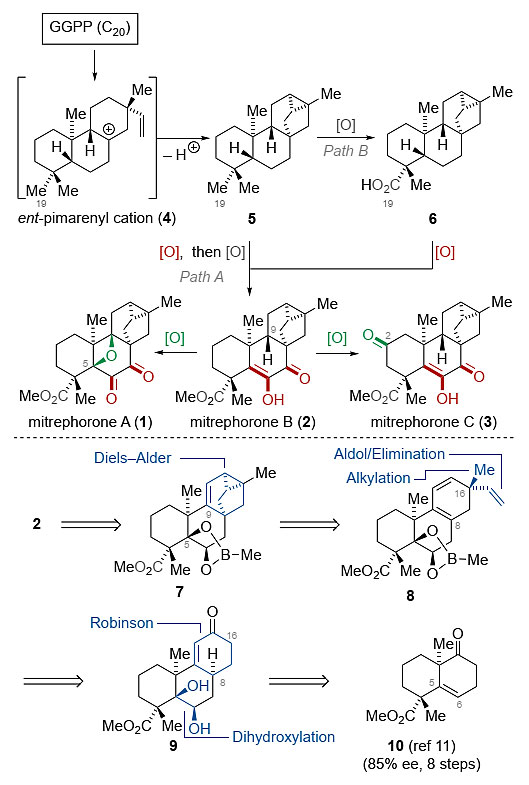
图1. Mitrephorone A(1)、B(2)、C(3)的生源合成方法及逆合成分析。图片来源:J. Am. Chem. Soc.
逆合成分析思路如下:目标分子mitrephorone B(2)可以通过三环化合物-[3.2.1.02,7]Oct-3-ene 7合成,7可以由5-乙烯基-1,3-环己二烯8通过分子内Diels-Alder(IMDA)反应构建,8则由烯酮化合物9来制备,9可由化合物10通过Robinson环化和双羟化来构建,而10为文献已知的化合物。
具体合成路线如图2所示,按照文献方法实现了克级规模(4.4 g)的10的不对称合成,且总收率良好。新戊基烯烃的Upjohn双羟化反应极具挑战性,在室温下不反应。幸运的是,当向反应中加入添加剂1,4-二氮杂二环[2.2.2]辛烷(DABCO)时,并在90 °C高温下进行双羟化反应,得到了1,2-二醇11。C5-C6烯烃的早期双羟化反应使作者研究了亲核取代对氧杂环丁烷形成的限制,并揭示了实现C-H键氧化的结构要求。11经两步Robinson环化转化为三环烯酮9,首先,11通过β-酮醛来活化(NaH、甲酸甲酯),随后该中间体与甲基乙烯基酮(MVK)在甲醇钠条件下,以良好的产率(两步产率57%)和优异的非对映选择性(20:1)得到9。
在C16处实现进一步的官能团化同时构建季碳中心需要保护1,2-二醇。通过对保护基(如二烷基硅烯、丙酮叉、苯亚甲基乙缩醛、环碳酸酯)进行筛选,作者发现一种很少使用的环硼酸酯是唯一的选择(MeB(OH)2、苯、30 °C)。该硼酸酯具有较高的稳定性,可进行后续的烷基化/Aldol反应,并可在后期进行选择性脱除。尽管α-甲基化(LiHMDS、MeI、82%)能够有效地进行,但是直接实现α-乙烯基化却导致了复杂的反应混合物和较低的分离产率。因此,作者采用了两步的方法。首先,与乙醛发生Aldol 反应(LDA、TMEDA、乙醛、-78 °C)得到12,经Martin sulfurane脱水和Luche还原得到相应的烯丙醇13,随后在23 °C以及对甲苯磺酸(40 mol%)的作用下,通过消除反应得到所需的5-乙烯基-1,3-环己烯8(产率96%)。随后在170 °C下进行Diels-Alder反应,以98%的产率得到7,该步的关键在于将消除与环加成步骤分开,因为环丙烷开环后,在高温和酸存在的条件下会放出乙烯并芳构化得到14。值得注意的是,最近在从Burmese amber中分离出的天然产物中也发现了已形成的碳环骨架,这引起了关于它们生物合成起源的思考。为了实现环硼酸酯的脱保护,7在KHF2(20.0 equiv.)的作用下得到二醇15,产率47%。将剩余的原料回收(39%),继续投入反应,经过三次循环以72%的总收率得到15,这使作者得以研究基于亲核取代的氧杂环丁烷的形成方法。然而,二醇15或其C6-酮衍生物通过质子化、卤化或C9-C11烯烃的环氧化引发的闭环反应都以失败告终。在大多数情况下,未反应的原料能够回收,但是在更剧烈的条件下底物则会分解。
对于15的选择性烯烃还原,作者采用了Shenvi课题组报道的直接氢原子转移(HAT)方法(J. Am. Chem. Soc., 2014, 136, 1300–1303)。在此条件下(Mn(dpm)3、PhSiH3、t-BuOOH、23 °C),环丙烷不发生氢解反应,在C9处以单一对映体的形式分离得到化合物16(产率为75%),同时伴随着少量的非对映体三醇化合物17(22%)。接着16经Ley氧化(TPAP、NMO、4 Å分子筛)得到18(产率77%),用二碘化钐脱去叔醇(产率为74%),并安装1,2二酮(SeO2、100 °C、1,4-二氧六环)得到mitrephorone B(2)。随后,作者测试了生物诱导C–H键氧化合成1的可行性。mitrephorone B(2)在White-Chen催化剂体系(25 mol% Fe(R,R)-PDP、H2O2、AcOH、MeCN、23 °C、1 h)下,以60%的产率得到mitrephorone A(1),这也是首次报道通过C–H键氧化形成氧杂环丁烷。使用对映体Fe(S,S)-PDP催化剂对该C-H键进行氧化,结果不匹配,仅获得了30%的mitrephorone A(1)。在没有铁催化剂的情况下,不发生氧化反应。此外,作者还通过Baran报道的电化学氧化法(J. Am. Chem. Soc., 2017, 139, 7448–7451)以49%的收率得到1。用光催化法(Angew. Chem. Int. Ed., 2018, 57, 4078–4082)也可以得到1,但收率显著降低,仅为14%。
作者发现,烯醇的存在对于氧杂环丁烷的形成至关重要。所有用α-羟基酮18合成氧杂环丁烷的方法都失败了,只观察到底物分解或原料回收。通过研究铁催化已知化合物20的C-H键氧化反应,作者进一步了解到,三醇17首先通过四步转化为19,将19置于TASF条件下可释放叔醇,并诱导互变异构化生成20。该中间体在White-Chen催化剂体系下,以13%的产率得到环化产物mitrephorone A(1)。氧杂环丁烷的选择性形成可能是由于烯醇的C5与H9(2.64 Å)之间的空间距离较短所致。与文献一致,这一过程是由烯酮氧化为三级自由基引起的。随后的氧掺入可能直接发生在C5位,或在自由基移位后,发生在C9位,这两种途径都可以发生氧杂环丁烷的闭环反应。

图2. Mitrephorone A(1)、B(2)的全合成。图片来源:J. Am. Chem. Soc.
总结
Thomas Magauer 教授课题组首次完成了ent-trachylobane类天然产物mitrephorone B(2)的不对称全合成,并受生源合成途径的启发,采用后期C-H键铁催化氧化或电化学氧化得到了mitrephorone A(1),这对于该类天然产物的全合成及多样性合成研究都具有重要的指导意义。然而,该方法仍存在一定的局限性,尽管作者对氧化剂进行了仔细的筛选,并且调研了结构相关的大量底物,在该条件下没能实现mitrephorone C(3)的合成。这说明,目前的C-H键氧化方法仍有局限,生源合成途径或许也需要进一步的深入研究。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Synthesis of (-)-Mitrephorone A via a Bio-inspired Late Stage C–H Oxidation of (-)-Mitrephorone B
Lukas Anton Wein, Klaus Wurst, Peter Angyal, Lara Weisheit, Thomas Magauer
J. Am. Chem. Soc., 2019, 141, 19589-19593, DOI: 10.1021/jacs.9b11646
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!




























 京公网安备 11010802027423号
京公网安备 11010802027423号