2-氧吲哚的酶催化合成
2-氧吲哚结构作为重要的药效基团存在于多种生物活性天然产物中,如抗肿瘤、HIV、疟疾、结核菌、氧化以及某些酶的抑制活性,用作酶抑制剂、神经保护剂、孕酮受体激动剂、抗癌药物、降血压药物等。含有该结构基团的化合物通常具有独特的生物活性,因而得到合成化学家的广泛研究,并获得一系列有价值的药物先导化合物或者临床药物,如舒尼替尼、NITD609、SM-130686和SAR405838等。
2-氧吲哚结构单元的化学合成方法很多,主要以靛红或其类似物为起始单元,通过一系列的化学反应转化而来,但是生物合成方法的研究很少,只有最近报道了两种生物合成的方法。一种是以黄素(FAD)为辅因子的单加氧酶催化氧化的方法,另一种是以血红素为辅因子的P450单加氧酶催化氧化的方法。这两种酶只能催化结构复杂的天然产物生物合成中间体,不能催化简单的吲哚衍生物发生氧化,合成相应的2-氧吲哚结构。上海交通大学的林双君教授(点击查看介绍)课题组于近期发现了一种以血红素为辅因子的色氨酸2,3-双加氧酶MarE,它可以催化一系列3-取代吲哚发生单加氧反应,生成2-氧吲哚结构,为2-氧吲哚的生物合成提供了有益的补充。
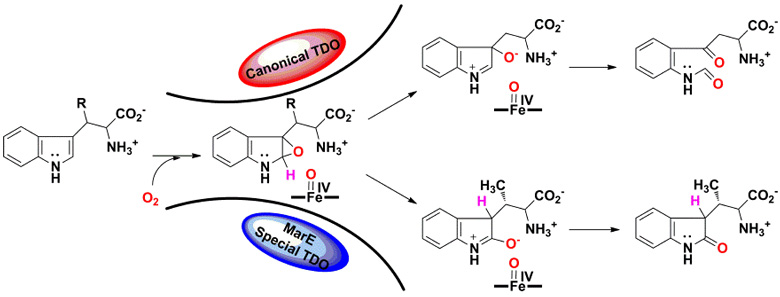
传统的色氨酸2,3-双加氧酶催化是将氧气分子的两个氧原子连续引入底物中,并伴随碳-碳键的断裂反应生成N-甲酰基犬尿酸,这是色氨酸代谢的第一步,也是速率控制步骤。林双君教授课题组发现的色氨酸2,3-双加氧酶MarE只将一个氧原子引入底物中,形成2-氧吲哚结构。该研究通过系统的体内遗传学和体外生物化学实验,确证了色氨酸2,3-双加氧酶MarE参与2-氧吲哚结构的形成;还通过一系列同位素标记实验推断该结构形成的化学机理;并通过序列对比、进化分析、蛋白特征鉴定等手段,证实MarE代表一类特殊的血红素依赖的色氨酸2,3-双加氧酶进化分支。同时,他们还发现MarE具有良好的底物适用性以及通过结构改造优化酶催化效率、开发为制备2-氧吲哚类化学品工具酶的潜力。
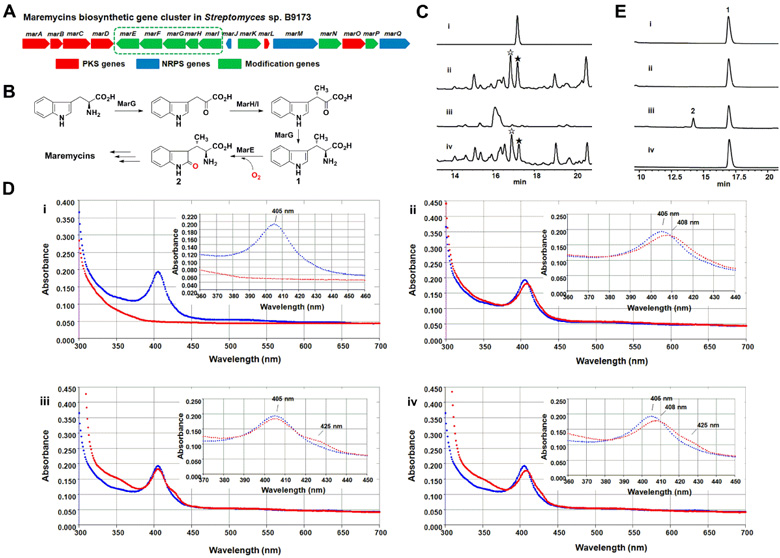
这一成果发表在J. Am. Chem. Soc. 上,文章的第一作者是上海交通大学的博士生张玉阳。
该论文作者为:Yuyang Zhang, Yi Zou, Nelson L. Brock, Tingting Huang, Yingxia Lan, Xiaozheng Wang, Zixin Deng, Yi Tang and Shuangjun Lin
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Characterization of 2-Oxindole Forming Heme Enzyme MarE, Expanding the Functional Diversity of the Tryptophan Dioxygenase Superfamily
J. Am. Chem. Soc., 2017, 139, 11887, DOI: 10.1021/jacs.7b05517
导师介绍
林双君
http://www.x-mol.com/university/faculty/48487
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!



























 京公网安备 11010802027423号
京公网安备 11010802027423号