灯泡可驱动的新型有机光动力纳米颗粒
光动力治疗在近些年的研究中受到了广泛的关注。与传统的肿瘤治疗相比,光动力治疗具有许多优点,例如高的时空分辨性、低的生理副作用、低的肿瘤耐药性等。由于近红外光具有深的组织穿透性,为了实现深层肿瘤组织中的光动力治疗,开发近红外区强吸收、高单线态氧量子效率的光敏剂是非常重要的。为了实现近红外光激发的光动力治疗,研究者利用稀土上转化纳米颗粒作为光转化介质,有效的吸收近红外光转化为可见光,进而活化稀土纳米颗粒表面的光敏剂。但是稀土上转化纳米颗粒存在许多不足,例如激发光功率较高、容易对生物组织造成光损伤、上转化量子效率低,并且稀土上转化纳米颗粒存在不确定的生理毒性,因此稀土掺杂的上转化纳米颗粒不适宜广泛的应用于临床转化。此外研究者开发出了卟啉、酞菁类大环光敏剂,但是这类光敏剂容易发生π-π堆积,淬灭了光敏剂的单线态氧产生能力。

图1.(a)近红外吸收的Car-BDP 纳米颗粒用于光动力治疗的示意图;(b)Car-BDP的光物理过程;(c)Car-BDP-TNM的结构示意图;(d)Car-BDP、PLA-PEG和PLA-PEG-FA分子结构。
近年来,麻省大学医学院的韩纲教授(点击查看介绍)设计两类新型灯泡可驱动的新型有机光动力纳米颗粒。第一类材料是咔唑乙烯基取代的碘化BODIPY光敏剂(Car-BDP),该光敏剂具有强的近红外光吸收和高的单线态氧量子效率。通过具有肿瘤靶向性的叶酸(Folic aicd, FA)的聚乳酸-聚乙二醇-叶酸(PLA-PEG-FA)包裹以后得到了具有肿瘤靶向性的纳米颗粒(Car-BDP-TNM),该纳米颗粒粒径均匀,并且在生理条件下稳定。Car-BDP-TNM有宽的近红外光吸收、高的单线态氧产生效率和良好的光稳定性。将Car-BDP-TNM应用于光动力治疗,家用卤素灯泡就可以有效地抑制在深层组织下肿瘤细胞的生长,而且对正常细胞具有较小的光损伤。
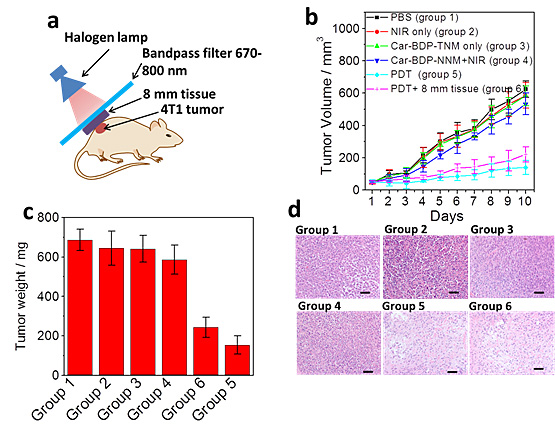
图2.(a)深层组织下的光动力治疗过程的示意图;(b)不同条件下光动力治疗后肿瘤体积大小的变化;(c)10天以后解剖分离下来的肿瘤组织的重量比较;(d)不同条件下肿瘤的H&E切片。照射光:670-800 nm,光强:12 mW/cm2。
Car-BDP-TNM具有近红外荧光发射,该特点可以实现精准的影像引导的光动力治疗。通过测试发现,Car-BDP-TNM的近红外荧光可以有效地对小鼠深层肿瘤原位检测。利用该特点,详细研究了Car-BDP-TNM在小鼠体内的肿瘤靶向性和在小鼠体内的代谢情况。与对照组相比,Car-BDP-TNM具有良好的肿瘤靶向性,经过24小时以后,Car-BDP-TNM在肿瘤组织部位进行有效的富集。对Car-BDP-TNM在各个器官的分布检测,最终发现Car-BDP-TNM可以通过肝脏组织代谢,排出体外,从而减少Car-BDP-TNM在小鼠体内的长时间的光毒性。
最后测定了Car-BDP-TNM对小鼠乳腺癌的光动力治疗效果。Car-BDP-TNM不仅对表层的肿瘤具有良好地肿瘤治疗效果,而且对深层的肿瘤也有很好的抑制作用。并且在治疗过程中,Car-BDP-TNM不会对小鼠的生长造成严重的影响。通过对主要器官的H&E切片分析,没有观察到对主要器官的损伤。通过对小鼠的长时间的血液分析,说明Car-BDP-TNM不会引发发炎症状。最后对Car-BDP-TNM在小鼠血液中残余量测定,进一步的证明,Car-BDP-TNM可以被小鼠排出体外。综上所述,Car-BDP-TNM是一种对方便廉价的深层肿瘤有抑制效果的光动力治疗试剂,将来在临床转化方面具有很大的潜力。
该项研究成果发表在J. Am. Chem. Soc. 杂志上。[1]
为了增强光敏剂在红区的吸收,提高光敏剂的单线态氧产生速率。韩纲教授和同事们近来利用共振能量转移原理,设计了另一类近红外超敏感纳米颗粒。

图3. (a)RET-BDP-TNM在小鼠肿瘤模型的光动力治疗示意图;(b) RET-BDP的光物理过程;(c)RET-BDP的分子结构。
通常共振能量转移里包含两个好的发光单元用于发光。那么一个好的发光单元和一个坏的发光单元(好的产生单线态氧的光敏剂)连接会怎么样呢?结果发现在该化合物中,激发给体时传递能量不再用于发光,但有效的转移给光敏剂受体最大限度产生单线态氧用于光动力治疗。利用这种方法,有效地拓宽了BODIPY光敏剂在近红外区的吸收范围,提高了BODIPY光敏剂在近红外区的吸收强度和单线态氧产生效率。通过靶向性的F-127-FA聚合物包裹以后,有效地将光敏剂分散在水中形成了粒径均匀的超小纳米颗粒(RET-BDP-TNM),并且该纳米颗粒在生理条件下具有良好的稳定性。RET-BDP-TNM在红区有宽谱吸收、单线态氧产生效率高和光稳定性良好,因此可将RET-BDP-TNM应用于光动力治疗。在细胞层面发现,RET-BDP-TNM与传统单发色团光敏剂相比,具有更加优异的光动力治疗效果。这说明利用共振能量转移原理可以有效增强光动力治疗中光敏剂的性能。
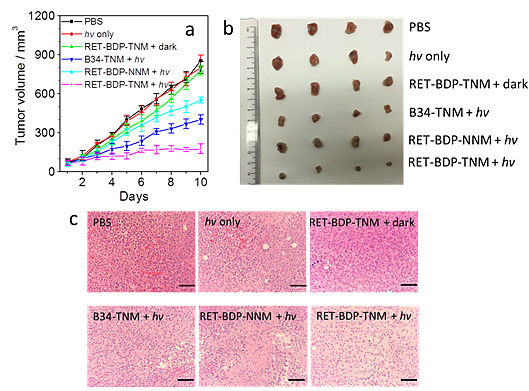
图4.(a)不同条件下小鼠乳腺癌肿瘤体积的变化;(b)小鼠肿瘤组织的大小比较图;(c)红木素伊红染色切片分析不同条件下肿瘤细胞的凋亡情况,标尺为50 μm。
RET-BDP-TNM不仅在细胞实验表现出良好的光动力治疗效果,而且还在小鼠乳腺癌的治疗方面也有良好表现。通过对RET-BDP-TNM的肿瘤靶向性测试,发现RET-BDP-TNM能够有效地在肿瘤组织部位富集,并且伴随着时间的延长可以有效的排出体外,这样可以避免RET-BDP-TNM在小鼠体内长时间的积累,降低RET-BDP-TNM的生理毒性。利用低功率的红光LED照射,发现RET-BDP-TNM能够有效的抑制小鼠乳腺癌的生长,与单发色团BODIPY光敏剂相比,肿瘤的抑制效果明显增强。这一结果说明,共振能量转移原理可以有效拓宽光敏剂的近红外区吸收,提高光敏剂单线态氧产生速率和光动力治疗的效果。最后分析了RET-BDP-TNM的潜在毒性和副作用,实验证明RET-BDP-TNM生理毒性低,不会对小鼠的主要器官造成严重的影响,因此RET-BDP-TNM在将来的临床转化方面具有一定的潜力。
该项研究成果发表在 Advanced Materials,并被选为封面文章。[2]
1. 该论文作者为:Ling Huang, Zhanjun Li, Yang Zhao, Yuanwei Zhang, Shuang Wu, Jianzhang Zhao, Gang Han
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Ultralow-Power Near Infrared Lamp Light Operable Targeted Organic Nanoparticle Photodynamic Therapy
J. Am. Chem. Soc., 2016, 138, 14586-14591, DOI: 10.1021/jacs.6b05390
2. 该论文作者为:Ling Huang, Zhanjun Li, Yang Zhao, Jinyi Yang, Yucheng Yang, Aarushi Iris Pendharkar, Yuanwei Zhang, Sharon Kelmar, Liyong Chen, Wenting Wu, Jianzhang Zhao, Gang Han
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Enhancing Photodynamic Therapy through Resonance Energy Transfer Constructed Near-Infrared Photosensitized Nanoparticles
Adv. Mater., 2017, 29, 1604789, DOI: 10.1002/adma.201604789
导师介绍
韩纲
http://www.x-mol.com/university/faculty/48467
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!




























 京公网安备 11010802027423号
京公网安备 11010802027423号