题目: 近红外光热纳米酶的冷冻强化微针用于角膜炎治疗
期刊:Nano Today
原文链接:https://doi.org/10.1016/j.nantod.2023.102000
IF:17.4
汇报人:韩希美2022级硕士

在本文中,我们提出了一种新型的纳米酶负载冷冻增强微针(FR-MNs),它能够在角膜内可控地递送纳米酶来治疗角膜炎。由铁离子、单宁酸(TA)和聚乙烯基吡咯烷酮构成的纳米酶;PVP) (FeTAP)被整合到MNs尖端中。冷冻过程可以大大提高尖端的机械强度。利用FeTAP的pH依赖性过氧化物酶模拟活性,FeTAP集成MNs可以在酸性条件下催化过氧化氢(H2O2)产生更多的氧化羟基(•OH)来杀死细菌。同时,FeTAP优异的光热效率可以进一步增强近红外(NIR)照射下的细菌杀灭能力。此外,光热作用可以迅速提高冷冻微针的温度,并在穿透后使MNs软化,从而使MNs更好地适应软组织。基于纳米酶负载的FR-MNs,我们已经证明,与传统滴眼液相比,该配方在大鼠眼睛感染模型中表现出更好的治疗潜力。这些特点赋予纳米酶负载FR-MNs具有巨大的科学价值和临床应用前景。

细菌性角膜炎又称细菌性角膜溃疡,是由葡萄球菌、链球菌、链球菌、假单胞菌等细菌感染引起的一种角膜炎症。细菌性角膜炎治疗不当或无效可能导致角膜穿孔、眼内感染,最终导致不可逆的视力损害和失明。抗生素滴眼液是治疗细菌性角膜炎最广泛使用的疗法。然而,由于角膜具有独特的解剖、生理、结构特征,如上皮内紧密连接等,滴眼液内药物局部给药后释放迅速,耐药时间短,生物利用度差。此外,抗生素的滥用导致抗生素耐药细菌的出现,使抗生素治疗的未来蒙上阴影。而传统的皮下针眼内注射可穿透表面屏障,改善局部给药,耐药时间长,但由于疼痛、就诊频繁、感染出血风险大,患者依从性较差。因此,对于治疗细菌性角膜炎,高度期待局部、持久和高效的抗菌药物的眼部输送,以及良好的患者依从性。
在此,我们提出了一种装载近红外(NIR)光热纳米酶的新型冷冻增强微针(FR-MNs)用于角膜炎治疗,如图1所示。纳米酶是指具有类似酶活性的纳米材料。由于纳米酶易于制备,催化活性可调节,稳定性高,成本效益高,易于处理,在各种应用中已成为天然酶的有希望的替代品。具体来说,由铁离子和多羟基苯酚组装的纳米酶表现出优异的生物相容性、生物降解性、ph依赖性催化活性和活性氧(ROS)形成或清除能力。然而,将这些纳米酶有效地局部递送到眼表仍然是一个挑战。或者,微针(MNs)是一组微米级的微小针头,广泛用于穿透表皮,实现无痛、无创、高效的透皮给药。药物、功能性细胞因子、干细胞、蛋白质、二维材料和金属-有机框架材料已被纳入MNs中,用于各种治疗目的。然而,一些天然聚合物制成的纳米粒子系统太软,无法达到足够的组织穿透强度。因此,如何提高机械强度,使纳米颗粒既能穿透组织,又能在穿透后实现自适应软化,是纳米颗粒应用于软组织的难点。

图1 原理图显示FR-MNs的组成及其在治疗角膜炎中的应用

1. FR-MNs制备与表征
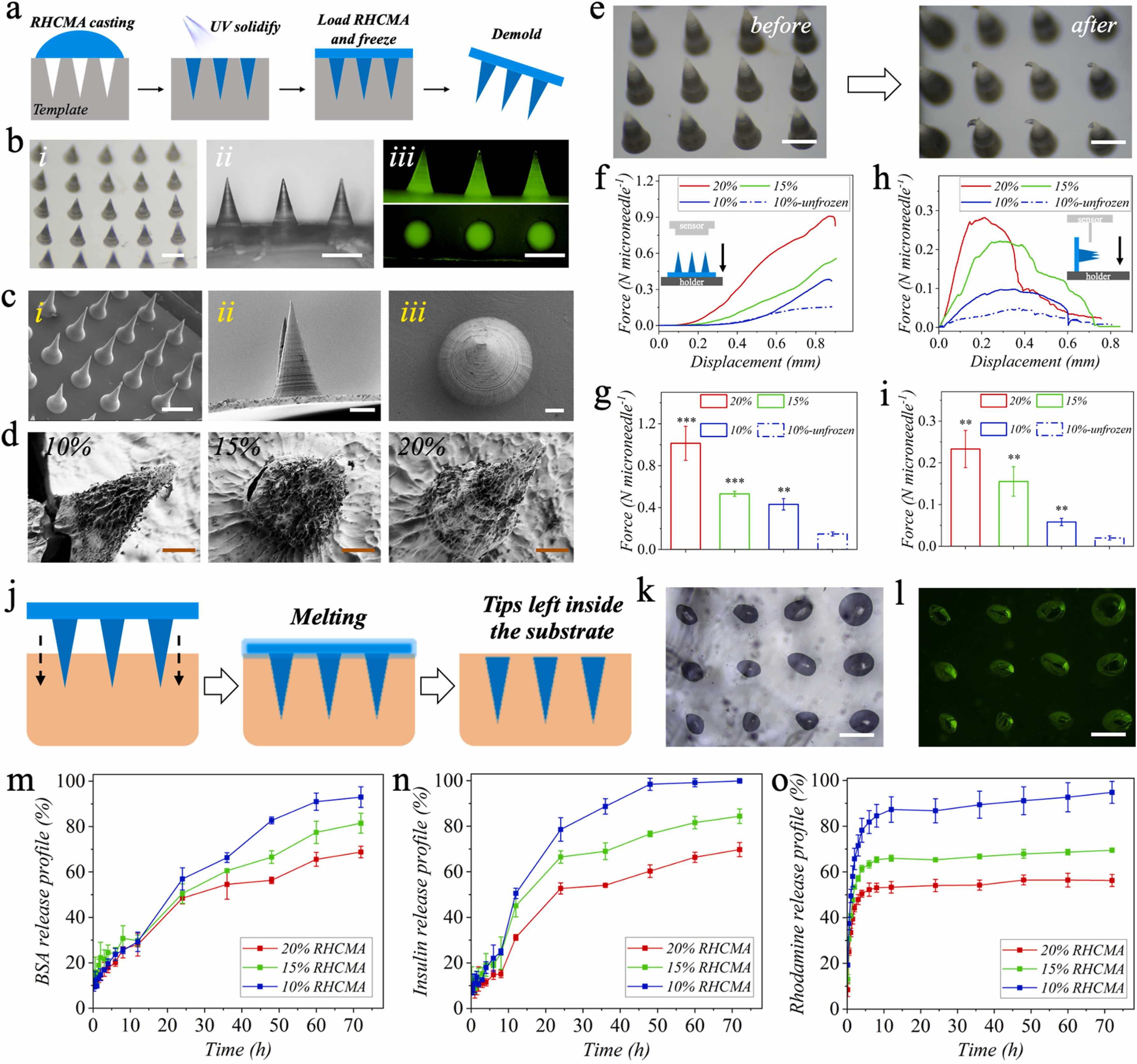
图2 FR-MNs的制备与表征。a) FR-MNs制备工艺示意图。b) FR-MNs的数字(i, ii)和荧光(iii)图像。c)不同侧视图下FR-MNs的SEM图像。d)不同RHCMA浓度制备的冷冻干燥FR-MNs的SEM图像。e)压缩前后的MNs数字图像。f, g)不同FR-MNs和未冻结MNs的压缩曲线和受力。h, i)不同FR-MNs和未冻结MNs的剪切曲线和受力。(n = 3,生物独立样本)。数据以mean±SD表示。j) FR-MNs渗入基体的过程示意图。k)琼脂糖被纳米粒子穿透后的数字和l)荧光图像。在不同FR-MNs中释放m) BSA, n)胰岛素和o) RhB。比例尺:500 μm in (b)、500 μm in、100 μm in、30 μm in (c、i)、ii、iii)、50 μm in (d)、500 μm in (e)、200 μm in (k)、(l)。
2. FeTAP纳米酶的表征
.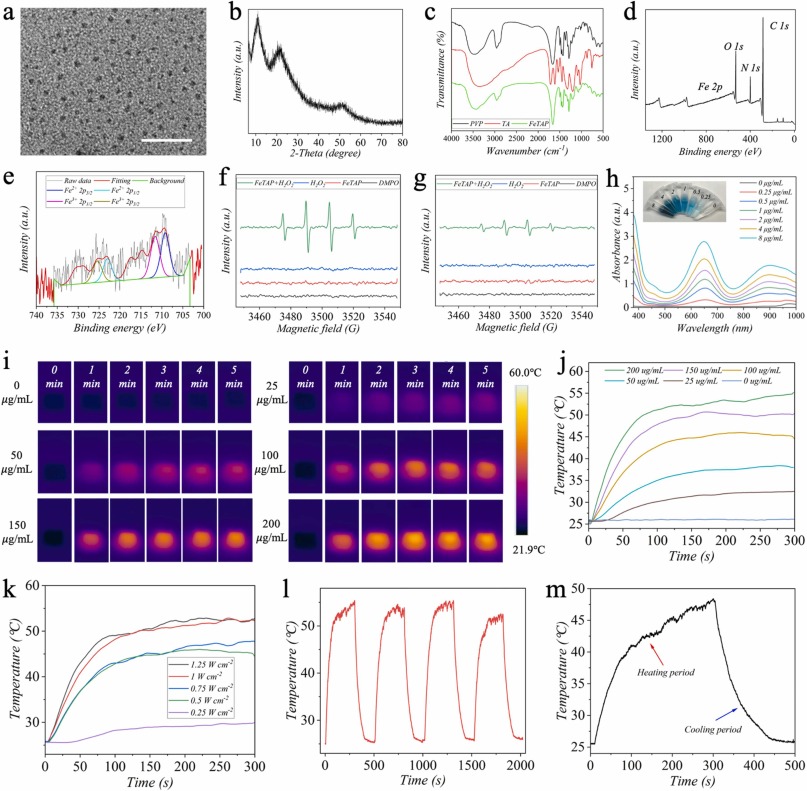
图3 FeTAP纳米酶的表征。a) FeTAP的TEM图像。b) FeTAP的XRD图谱。c) PVP、TA和FeTAP的FTIR光谱。d) FeTAP的XPS光谱。e) FeTAP的Fe2p XPS谱。f)酸性(pH=5.5)和g)中性(pH=7.4)条件下FeTAP、H2O2和FeTAP在H2O2存在下的ESR光谱。h)不同浓度FeTAP孵育TMBox后的吸光度曲线。所插入的图像是相应的颜色变化。结合FeTAP的MNs光热图像i)和加热曲线j)。k)不同辐照功率密度下掺入FeTAP的MNs的加热曲线。l) TeTAP的光热稳定性。m) FeTAP一次加热和冷却温度变化。比例尺:20nm in (a)。
3. FeTAP的体外抗菌作用

图4 FeTAP的体外抗菌作用。a)用缓冲液(对照)、H2O2、FeTAP和FeTAP+H2O2处理后的细菌的琼脂平板照片,有或没有近红外照射。b)与(a)相同处理后细菌的SEM图像。与(a)相同处理后c)金黄色葡萄球菌和d)大肠杆菌的荧光活/死图像。e)金黄色葡萄球菌的生存能力。f)大肠杆菌的生存能力。比例尺:金黄色葡萄球菌1 μm (b),大肠杆菌2 μm (b), 50 μm (c, d)。* p<0.05, ** p<0.01, *** p<0.001,组间比较;### p <0.001,组间比较。
4. 负载FeTAP的MNs对角膜细胞的影响

图5 负载FeTAP的MNs对角膜细胞的影响。a) HKs和HCECs在对照、MNs和不同浓度FeTAP的MNs中培养3天后的活/死染色图像。b) HCECs和c) HKs在培养1、2、3天后的细胞活力。HKs和HCECs中d) ALDH3A1和e) CK12的免疫荧光染色。比例尺:200 μ in (a)、100 μ in (d、e)。
5. 负载FeTAP的FR-MNs的体内抗菌评价

图6 负载FeTAP的FR-MNs的体内抗菌评价。a)不同时间滴眼液、FR-MNs、FeTAP + FR-MNs和FeTAP + FR-MNs + NIR处理感染角膜的代表性照片。b)经(a)相同处理后感染角膜细菌的琼脂平板照片。c)第1天和第7天细菌数量直方图。d) (a)中相同处理后7天感染角膜的代表性HE染色图像。e) (a)中相同处理后7天感染角膜的角膜上皮和间质厚度。比例尺:放大图1.5 mm in (a), 100 μ in (d), 50 μm。
6. 免疫染色验证FR-MNs负载FeTAP的抗菌评价。

图7 免疫染色验证FeTAP负载FR-MNs的抗菌评价。具有代表性的免疫荧光a) TNF-α, b) IL-6和免疫组织化学c) CD68, d)滴剂、FR-MNs、FeTAP + FR-MNs和FeTAP + FR-MNs + NIR处理7天后感染角膜的VEGF染色图像。e) TNF-α阳性细胞,f) IL-6阳性细胞,g) CD68 MFI, h) VEGF MFI直方图。比例尺:100 μm in (a-d),放大图50 μm。* p<0.05, ** p <0.01, *** p<0.001。

总之,我们提出了负载纳米酶的冷冻强化微针,能够在角膜内可控地递送纳米酶来治疗角膜炎。冷冻过程可以显著增强FR-MNs的机械强度,并且在FR-MNs中观察到不同分子量分子的可控释放。FeTAP能在酸性条件下催化H2O2产生更多的•OH,从而杀死细菌。同时,FeTAP优异的光热效率可以进一步增强近红外照射下的杀菌能力。此外,FeTAP负载的MNs对HKs和HCECs具有良好的生物相容性。值得注意的是,与传统滴眼液相比,该配方在大鼠眼睛感染模型中表现出更好的治疗潜力。这些特点赋予了纳米酶负载FR-MNs具有巨大的科学价值和临床应用前景。
