当前位置:
X-MOL 学术
›
Cell Chem. Bio.
›
论文详情
Our official English website, www.x-mol.net, welcomes your feedback! (Note: you will need to create a separate account there.)
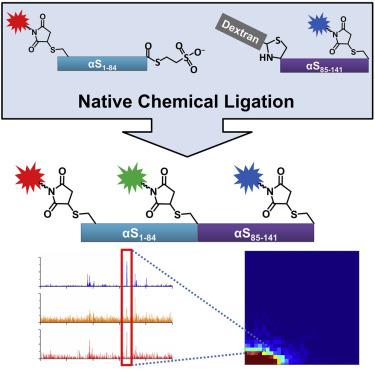
Site-Specific Three-Color Labeling of α-Synuclein via Conjugation to Uniquely Reactive Cysteines during Assembly by Native Chemical Ligation
Cell Chemical Biology ( IF 8.6 ) Pub Date : 2018-04-19 , DOI: 10.1016/j.chembiol.2018.03.009 Taehyung C. Lee , Crystal R. Moran , Philip A. Cistrone , Philip E. Dawson , Ashok A. Deniz
Cell Chemical Biology ( IF 8.6 ) Pub Date : 2018-04-19 , DOI: 10.1016/j.chembiol.2018.03.009 Taehyung C. Lee , Crystal R. Moran , Philip A. Cistrone , Philip E. Dawson , Ashok A. Deniz
|
Single-molecule fluorescence is widely used to study conformational complexity in proteins, and has proven especially valuable with intrinsically disordered proteins (IDPs). Protein studies using dual-color single-molecule Förster resonance energy transfer (smFRET) are now quite common, but many could benefit from simultaneous measurement of multiple distances through multi-color labeling. Such studies, however, have suffered from limitations in site-specific incorporation of more than two dyes per polypeptide. Here we present a fully site-specific three-color labeling scheme for α-synuclein, an IDP with important putative functions and links to Parkinson disease. The convergent synthesis combines native chemical ligation with regiospecific cysteine protection of expressed protein fragments to permit highly controlled labeling via standard cysteine-maleimide chemistry, enabling more global smFRET studies. Furthermore, this modular approach is generally compatible with recombinant proteins and expandable to accommodate even more complex experiments, such as by labeling with additional colors.
中文翻译:

通过天然化学连接组装过程中通过缀合到唯一反应性半胱氨酸的α-突触核蛋白的特定位点三色标记
单分子荧光被广泛用于研究蛋白质的构象复杂性,并已被证明对固有无序蛋白质(IDP)尤其有价值。现在,使用双色单分子Förster共振能量转移(smFRET)进行蛋白质研究非常普遍,但是许多人可以通过多色标记同时测量多个距离而受益。然而,这些研究在每个多肽多于两种染料的位点特异性掺入方面受到限制。在这里,我们为α-突触核蛋白(一种具有重要推定功能并与帕金森氏病有联系的IDP)提供了一个完全针对特定部位的三色标记方案。融合合成将天然化学连接与表达蛋白片段的区域特异性半胱氨酸保护结合在一起,以允许通过标准半胱氨酸-马来酰亚胺化学进行高度受控的标记,从而实现了更多的全球smFRET研究。此外,这种模块化方法通常与重组蛋白兼容,并且可以扩展以适应更复杂的实验,例如通过标记其他颜色。
更新日期:2018-06-22
中文翻译:

通过天然化学连接组装过程中通过缀合到唯一反应性半胱氨酸的α-突触核蛋白的特定位点三色标记
单分子荧光被广泛用于研究蛋白质的构象复杂性,并已被证明对固有无序蛋白质(IDP)尤其有价值。现在,使用双色单分子Förster共振能量转移(smFRET)进行蛋白质研究非常普遍,但是许多人可以通过多色标记同时测量多个距离而受益。然而,这些研究在每个多肽多于两种染料的位点特异性掺入方面受到限制。在这里,我们为α-突触核蛋白(一种具有重要推定功能并与帕金森氏病有联系的IDP)提供了一个完全针对特定部位的三色标记方案。融合合成将天然化学连接与表达蛋白片段的区域特异性半胱氨酸保护结合在一起,以允许通过标准半胱氨酸-马来酰亚胺化学进行高度受控的标记,从而实现了更多的全球smFRET研究。此外,这种模块化方法通常与重组蛋白兼容,并且可以扩展以适应更复杂的实验,例如通过标记其他颜色。

























 京公网安备 11010802027423号
京公网安备 11010802027423号