当前位置:
X-MOL 学术
›
Bioconjugate Chem.
›
论文详情
Our official English website, www.x-mol.net, welcomes your feedback! (Note: you will need to create a separate account there.)
Self-Transfecting Micellar RNA: Modulating Nanoparticle Cell Interactions via High Density Display of Small Molecule Ligands on Micelle Coronas
Bioconjugate Chemistry ( IF 4.7 ) Pub Date : 2017-12-29 00:00:00 , DOI: 10.1021/acs.bioconjchem.7b00657 Alexander Roloff , David A. Nelles , Matthew P. Thompson , Gene W. Yeo , Nathan C. Gianneschi 1
Bioconjugate Chemistry ( IF 4.7 ) Pub Date : 2017-12-29 00:00:00 , DOI: 10.1021/acs.bioconjchem.7b00657 Alexander Roloff , David A. Nelles , Matthew P. Thompson , Gene W. Yeo , Nathan C. Gianneschi 1
Affiliation
|
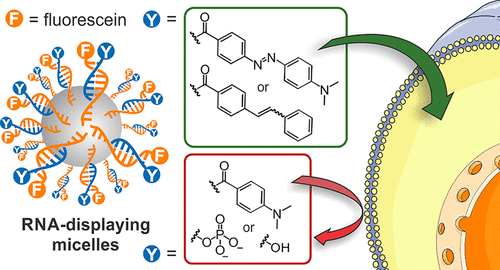
The intracellular delivery of synthetic nucleic acids represents a major challenge in biotechnology and in biomedicine. Methods to deliver short, double-stranded RNA to living cells are of particular interest because of the potential to engage the RNA interference machinery and to regulate mRNA expression. In this work, we describe novel RNA-polymer amphiphiles that assemble into spherical micellar nanoparticles with diameters of ca. 15–30 nm and efficiently enter live cells without transfection reagents. Each micelle consists of approximately 100 RNA strands forming a densely packed corona around a polymeric core. Importantly, the surface-displayed RNA remains accessible for hybridization with complementary RNA. Chemical modification of the termini of hybridized RNA strands enabled the display of small organic moieties on the outer surface of the micelle corona. We found that some of these modifications can have a tremendous impact on cellular internalization efficiencies. The display of hydrophobic dabcyl or stilbene units dramatically increased cell uptake, whereas hydrophilic neutral hydroxy or anionic phosphate residues were ineffective. Interestingly, neither of these modifications mediated noticeable uptake of free RNA oligonucleotides. We infer that their high density display on micellar nanoparticle surfaces is key for the observed effect; achieved with local effective surface concentrations in the millimolar range. We speculate that weak interactions with cell surface receptors that are amplified by the multivalent presentation of such modifications may be responsible. The installation of small molecule ligands on nanomaterial surfaces via hybridization of chemically modified oligonucleotides offers a simple and straightforward way to modulate cellular uptake of nanoparticles. Biological functionality of micellar RNA was demonstrated through the sequence-specific regulation of mRNA expression in HeLa cells.
中文翻译:

自我转染的胶束RNA:通过高密度展示的小分子配体在Micelle电晕上调节纳米颗粒细胞相互作用。
合成核酸的细胞内递送代表了生物技术和生物医学中的主要挑战。方法以短交付,双链RNA活细胞是由于潜在的特别感兴趣的参与RNA干扰机制和规范米RNA表达。在这项工作中,我们描述了新颖的RNA聚合物两亲物,它们组装成直径约为ca的球形胶束纳米颗粒。15–30 nm,无需转染试剂即可有效进入活细胞。每个胶束由大约100条RNA链组成,在聚合物核周围形成密集堆积的电晕。重要的是,表面展示的RNA仍可与互补RNA杂交。杂交RNA链末端的化学修饰使得在胶束电晕的外表面上可以显示出小的有机部分。我们发现这些修饰中的一些可以对细胞内在化效率产生巨大影响。疏水的dabcyl或1,2-二苯乙烯单元的展示极大地增加了细胞摄取,而亲水性中性羟基或阴离子磷酸酯残基无效。有趣的是,这些修饰均未介导游离RNA寡核苷酸的明显摄取。我们推断它们在胶束纳米颗粒表面上的高密度显示是观察到的效果的关键。局部有效表面浓度在毫摩尔范围内即可达到。我们推测与细胞表面受体的弱相互作用可能是由这种修饰的多价呈现所放大的。通过化学修饰的寡核苷酸杂交将小分子配体安装在纳米材料表面上,提供了一种简单直接的方法来调节细胞对纳米颗粒的吸收。胶束RNA的生物学功能通过序列特异性调控 有趣的是,这些修饰均未介导游离RNA寡核苷酸的明显摄取。我们推断它们在胶束纳米颗粒表面上的高密度显示是观察到的效果的关键。局部有效表面浓度在毫摩尔范围内即可达到。我们推测与细胞表面受体的弱相互作用可能是由这种修饰的多价呈现所放大的。通过化学修饰的寡核苷酸杂交将小分子配体安装在纳米材料表面上,提供了一种简单直接的方法来调节细胞对纳米颗粒的吸收。胶束RNA的生物学功能通过序列特异性调控 有趣的是,这些修饰均未介导游离RNA寡核苷酸的明显摄取。我们推断它们在胶束纳米颗粒表面上的高密度显示是观察到的效果的关键。局部有效表面浓度在毫摩尔范围内即可达到。我们推测与细胞表面受体的弱相互作用可能是由这种修饰的多价呈现所放大的。通过化学修饰的寡核苷酸杂交将小分子配体安装在纳米材料表面上,提供了一种简单直接的方法来调节细胞对纳米颗粒的吸收。胶束RNA的生物学功能通过序列特异性调控 我们推断它们在胶束纳米颗粒表面上的高密度显示是观察到的效果的关键。局部有效表面浓度在毫摩尔范围内即可达到。我们推测与细胞表面受体的弱相互作用可能是由这种修饰的多价呈现所放大的。通过化学修饰的寡核苷酸杂交将小分子配体安装在纳米材料表面上,提供了一种简单直接的方法来调节细胞对纳米颗粒的摄取。胶束RNA的生物学功能通过序列特异性调控 我们推断它们在胶束纳米颗粒表面上的高密度显示是观察到的效果的关键。局部有效表面浓度在毫摩尔范围内即可达到。我们推测与细胞表面受体的弱相互作用可能是由这种修饰的多价呈现所放大的。通过化学修饰的寡核苷酸杂交将小分子配体安装在纳米材料表面上,提供了一种简单直接的方法来调节细胞对纳米颗粒的吸收。胶束RNA的生物学功能通过序列特异性调控 我们推测与细胞表面受体的弱相互作用可能是由这种修饰的多价呈现所放大的。通过化学修饰的寡核苷酸杂交将小分子配体安装在纳米材料表面上,提供了一种简单直接的方法来调节细胞对纳米颗粒的吸收。胶束RNA的生物学功能通过序列特异性调控 我们推测与细胞表面受体的弱相互作用可能是由这种修饰的多价呈现所放大的。通过化学修饰的寡核苷酸杂交将小分子配体安装在纳米材料表面上,提供了一种简单直接的方法来调节细胞对纳米颗粒的吸收。胶束RNA的生物学功能通过序列特异性调控HeLa细胞中的m RNA表达。
更新日期:2017-12-29
中文翻译:

自我转染的胶束RNA:通过高密度展示的小分子配体在Micelle电晕上调节纳米颗粒细胞相互作用。
合成核酸的细胞内递送代表了生物技术和生物医学中的主要挑战。方法以短交付,双链RNA活细胞是由于潜在的特别感兴趣的参与RNA干扰机制和规范米RNA表达。在这项工作中,我们描述了新颖的RNA聚合物两亲物,它们组装成直径约为ca的球形胶束纳米颗粒。15–30 nm,无需转染试剂即可有效进入活细胞。每个胶束由大约100条RNA链组成,在聚合物核周围形成密集堆积的电晕。重要的是,表面展示的RNA仍可与互补RNA杂交。杂交RNA链末端的化学修饰使得在胶束电晕的外表面上可以显示出小的有机部分。我们发现这些修饰中的一些可以对细胞内在化效率产生巨大影响。疏水的dabcyl或1,2-二苯乙烯单元的展示极大地增加了细胞摄取,而亲水性中性羟基或阴离子磷酸酯残基无效。有趣的是,这些修饰均未介导游离RNA寡核苷酸的明显摄取。我们推断它们在胶束纳米颗粒表面上的高密度显示是观察到的效果的关键。局部有效表面浓度在毫摩尔范围内即可达到。我们推测与细胞表面受体的弱相互作用可能是由这种修饰的多价呈现所放大的。通过化学修饰的寡核苷酸杂交将小分子配体安装在纳米材料表面上,提供了一种简单直接的方法来调节细胞对纳米颗粒的吸收。胶束RNA的生物学功能通过序列特异性调控 有趣的是,这些修饰均未介导游离RNA寡核苷酸的明显摄取。我们推断它们在胶束纳米颗粒表面上的高密度显示是观察到的效果的关键。局部有效表面浓度在毫摩尔范围内即可达到。我们推测与细胞表面受体的弱相互作用可能是由这种修饰的多价呈现所放大的。通过化学修饰的寡核苷酸杂交将小分子配体安装在纳米材料表面上,提供了一种简单直接的方法来调节细胞对纳米颗粒的吸收。胶束RNA的生物学功能通过序列特异性调控 有趣的是,这些修饰均未介导游离RNA寡核苷酸的明显摄取。我们推断它们在胶束纳米颗粒表面上的高密度显示是观察到的效果的关键。局部有效表面浓度在毫摩尔范围内即可达到。我们推测与细胞表面受体的弱相互作用可能是由这种修饰的多价呈现所放大的。通过化学修饰的寡核苷酸杂交将小分子配体安装在纳米材料表面上,提供了一种简单直接的方法来调节细胞对纳米颗粒的吸收。胶束RNA的生物学功能通过序列特异性调控 我们推断它们在胶束纳米颗粒表面上的高密度显示是观察到的效果的关键。局部有效表面浓度在毫摩尔范围内即可达到。我们推测与细胞表面受体的弱相互作用可能是由这种修饰的多价呈现所放大的。通过化学修饰的寡核苷酸杂交将小分子配体安装在纳米材料表面上,提供了一种简单直接的方法来调节细胞对纳米颗粒的摄取。胶束RNA的生物学功能通过序列特异性调控 我们推断它们在胶束纳米颗粒表面上的高密度显示是观察到的效果的关键。局部有效表面浓度在毫摩尔范围内即可达到。我们推测与细胞表面受体的弱相互作用可能是由这种修饰的多价呈现所放大的。通过化学修饰的寡核苷酸杂交将小分子配体安装在纳米材料表面上,提供了一种简单直接的方法来调节细胞对纳米颗粒的吸收。胶束RNA的生物学功能通过序列特异性调控 我们推测与细胞表面受体的弱相互作用可能是由这种修饰的多价呈现所放大的。通过化学修饰的寡核苷酸杂交将小分子配体安装在纳米材料表面上,提供了一种简单直接的方法来调节细胞对纳米颗粒的吸收。胶束RNA的生物学功能通过序列特异性调控 我们推测与细胞表面受体的弱相互作用可能是由这种修饰的多价呈现所放大的。通过化学修饰的寡核苷酸杂交将小分子配体安装在纳米材料表面上,提供了一种简单直接的方法来调节细胞对纳米颗粒的吸收。胶束RNA的生物学功能通过序列特异性调控HeLa细胞中的m RNA表达。


























 京公网安备 11010802027423号
京公网安备 11010802027423号