Stefan Matile课题组Angew:阴离子-π催化作用的Diels-Alder反应
π酸分子通过阴离子-π相互作用形成阴离子过渡态或反应中间体是一种新颖的非共价作用机制,在化学领域中的研究才刚刚起步。目前,人们已发展了不对称阴离子-π催化剂用于设计烯醇、烯胺、亚胺等底物参与的不对称反应,与此同时,阴离子-π酶和电场辅助的阴离子-π催化剂也相继报道。Diels-Alder反应是经典的协同环加成反应,以往该类反应通常以Lewis酸活化双烯体,人们也同时实现了碱催化5H-噁唑-4-酮、5H-噻唑-4-酮和3-羟基-2-吡喃酮等双烯体的Diels-Alder环加成过程。金鸡纳碱衍生的叔胺可作为有机分子催化剂用于活化以上三种双烯体,与其他亲双烯体结合产生高endo选择性和对映选择性的环加成产物。然而选择性合成exo构型的环加成产物却存在巨大的挑战。
最近,瑞士日内瓦大学的Stefan Matile教授课题组对羟基吡喃酮、噁唑酮和噻唑酮等双烯体的Diels-Alder反应进行探究,这些分子可以经由阴离子二烯与不同环状或非环状的亲双烯体发生[4+2]环加成,得到具有四个新的立体中心的双环产物。他们利用萘二甲酰亚胺(NDI)及其π平面邻近位点修饰的氨基设计了一种双官能化催化剂,通过阴离子-π相互作用可以在π酸芳香环表面形成稳定的阴离子exo构型的过渡态,由此完成exo构型专一、高对映选择性的Diels-Alder反应,Michael加成等副反应可以得到很好的抑制。这些是利用常规的有机分子催化剂难以实现的,相关工作发表在Angew. Chem. Int. Ed. 上。

Stefan Matile教授。图片来源:University of Geneva
为了研究阴离子-π相互作用催化体系下Diels-Alder反应的选择性,作者设计并合成了如图1所示的6种阴离子-π催化剂,这些分子均由萘二甲酰亚胺(NDI)及其π平面邻近位点修饰的氨基构成,同时也合成了不含有π酸芳香环的对照催化剂7。
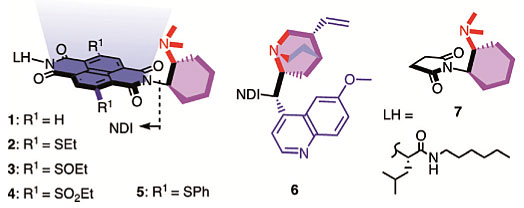
图1. 研究中所使用的阴离子-π催化剂。图片来源:Angew. Chem. Int. Ed.
作者首先选择5H-噁唑-4-酮8作为双烯体,研究与亲双烯体9的[4+2]环加成反应。在催化剂1-5的作用下,反应都能几乎以化学计量的产率得到exo构型Diels-Alder反应的产物10,非对映选择性大于20:1,对映选择性为84-99%。溴取代的9b参与反应得到的产物10b经X射线单晶衍射表征确定其为exo构型。仅催化剂6的催化效果不够理想。当催化剂1中的叔胺基团换成碱性更强的胍基时,立体选择性有所下降,这表明对于酸性较强的底物8,阴离子-π催化剂中碱性基团相对于π酸平面的位置对反应具有重要影响,相比之下,其碱性强弱则不占据主要影响因素。当他们选用对照催化剂7参与反应时,非对映选择性只有1.1:1,且对映选择性小于3%;选用常规的硫脲催化剂也只能得到endo型选择性的产物。这种exo型选择性与阴离子-π相互作用具有直接联系,底物8共轭碱离域的阴离子可通过该作用加以稳定,从而形成阴离子exo型[4+2]环加成反应过渡态。作者还提出exo型Diels-Alder反应的过渡态,在TS1中,受益于π-π相互作用,亲双烯体发生活化并从π平面接近二烯,并在整个反应中都保持稳定的阴离子-π相互作用。和endo型过渡态TS2相比,亲双烯体背离π平面,无法与π平面相互作用,导致环加成过程中阴离子-π相互作用降低,在能量上是不利的。
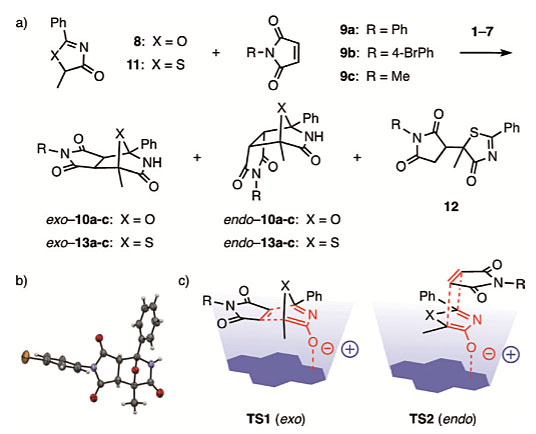
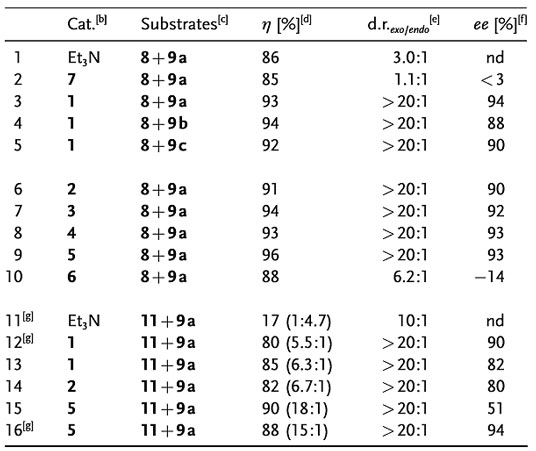
图2. 噁唑酮或噻唑酮作为负离子双烯体的[4+2]环加成反应。图片来源:Angew. Chem. Int. Ed.
他们还通过以下实验证实这一结论。当催化剂中NDI的π酸性增强时,反应的活化能降低,反应速率增加,并且得到exo型环加成产物的d.r.值和ee 值也相应增加。反应中加入抑制阴离子-π相互作用的四丁基硝酸铵会使产物的选择性下降。
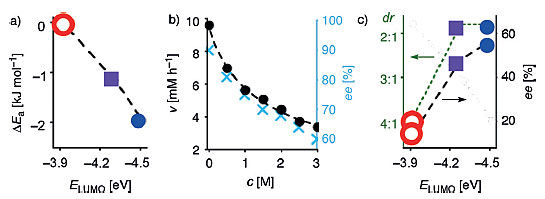
图3. 催化剂的π酸性对反应速率和选择性的影响。图片来源:Angew. Chem. Int. Ed.
以往的有机分子催化5H-噻唑-4-酮和马来酰亚胺反应主要得到Michael加成的产物12,当加入阴离子-π催化剂5时,则以绝对的优势获得环加成产物,图4a和4b中的蓝色特征峰预示着存在Michael加成产物,红色特征峰表示存在exo型Diels-Alder产物,绿色信号则与endo型Diels-Alder产物相关。由此可以看出,催化剂5在exo型Diels-Alder反应中具有非常重要的作用。
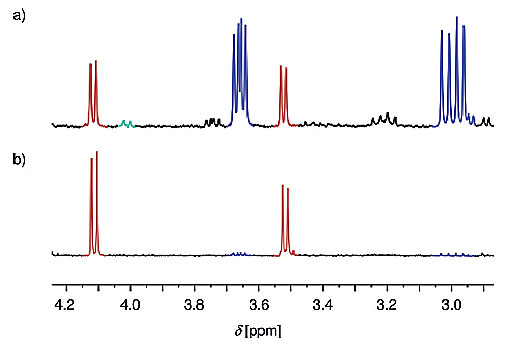
图4. 5H-噻唑-4-酮和马来酰亚胺反应后混合产物的NMR表征。图片来源:Angew. Chem. Int. Ed.
作者还尝试了3-羟基-2-吡喃酮14和富马酸二甲酯的Diels-Alder反应,得到反式的产物,而与马来酸二甲酯反应则全部生成顺式的产物,整个反应过程中并没有观察到Michael加成的产物和异构化产物,由此也证明了该反应经历了协同的[4+2]环加成过程。
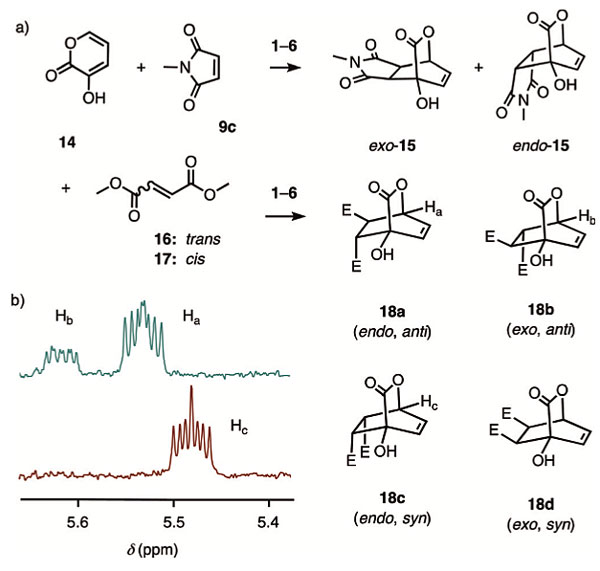
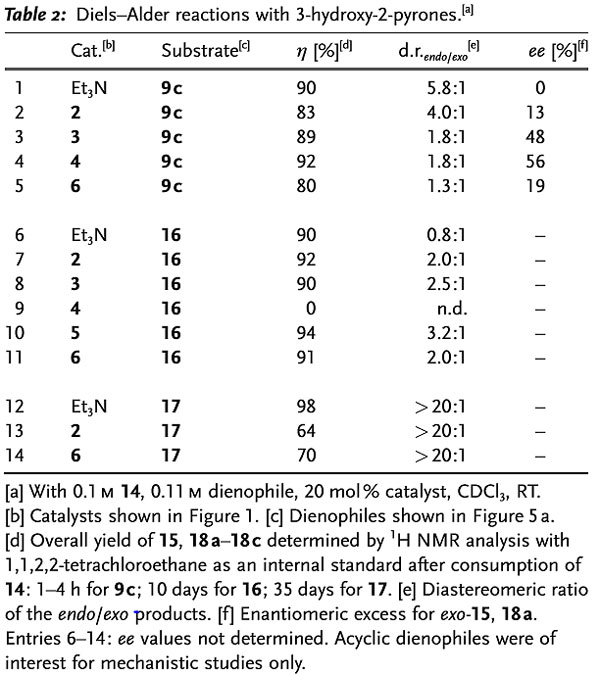
图5. 3-羟基-2-吡喃酮参与的Diels-Alder反应。图片来源:Angew. Chem. Int. Ed.
——总结——
Stefan Matile教授报道了一种双官能化的阴离子-π相互作用催化体系,催化剂由萘二甲酰亚胺(NDI)及其π平面邻近位点修饰的氨基组成,可以在π酸芳香环表面通过阴离子-π相互作用选择性地稳定exo反应过渡态,从而完成exo构型专一、高对映选择性的Diels-Alder反应,Michael加成等副反应可以得到很好的抑制。这种新型作用机制的催化剂对Diels-Alder反应选择性的有效调控在有机合成中具有重要的意义。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Anion–π Catalysis of Diels–Alder Reactions
Angew. Chem. Int. Ed., 2017, 56, 13066, DOI: 10.1002/anie.201707730
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!


























 京公网安备 11010802027423号
京公网安备 11010802027423号