Chem封面:溶液中阴离子识别主要依靠静电作用?
想必大家对主客体化学的概念并不陌生。主体最初是指人工合成的有机大环分子,客体往往是体积较小的离子或者分子,主客体之间依赖非共价的弱相互作用力进行可逆的识别。主客体化学在现代化学中又称为超分子化学,这门学科虽仍处于发展期,但其潜在的应用前景涵盖了其他化学学科不曾涉及的领域。其中一个著名的例子是分子机器,Sir J. Fraser Stoddart、Jean P. Sauvage以及Ben L. Feringa因为在分子机器领域的贡献而获得了2016年的诺贝尔化学奖。
笔者要跟大家探讨的是以阴离子为客体的超分子化学。阴离子较阳离子在以往很长一段时间被忽略。随着社会对可持续发展的需求日渐增加,阴离子的重要性得到超分子化学家们越来越多的认识和重视。阴离子广泛参与清洁能源、环境整治、农业和水资源生产,又与基础化学学科息息相关,例如有机分子催化、材料科学以及药物化学。
目前在主体的设计上化学家们大多采用尝试法。利用电脑辅助分子设计(Computer-Aided Design, CAD)虽然可以大大提高候选主体的数量从而提高理想主体的发现概率,但是目前化学家们还无法准确预测主客体在溶液中的结合自由能,这使得CAD这一现代技术不能在该领域发挥作用。今天给大家带来的故事可以说为CAD的应用打开了一扇大门,更是对阴离子主体投入实际应用提供了更多的可能。故事的分子主角,Triazolophane,是时任美国印第安纳大学布鲁明顿分校(Indiana University Bloomington)化学系助理教授的Amar H. Flood(图1)课题组在2008年发现合成的化合物。

图1. Amar H. Flood教授(右)获Cram Lehn Petersen奖。图片来源:Chem. Commun.
Triazolophane仅凭八个C–H键作为氢键给体(Angew. Chem. Int. Ed., 2008, 47, 2649,图2),其中四个被三唑极化,就可以对氯离子(Cl–)实现高强度(108 M–1)结合。这个强度相当于在1升的溶液里若存在2毫克以上的Triazolophane,它就可以与同浓度的Cl–离子达到90%以上的结合效率。

图2. Triazolophane对Cl–离子可以进行选择性高强度的识别。图片来源:Chem
2008年起,基于C–H氢键给体的阴离子识别成为这一领域的热门主体设计元素。Flood教授在该领域更是持续地做出重要发现(例如J. Am. Chem. Soc., 2013, 136, 14401; Nat. Chem., 2013, 5, 704; J. Am. Chem. Soc., 2014, 137, 5078; Angew. Chem. Int. Ed., 2016, 55, 14057)。Flood教授现任印第安纳大学化学系的研究生教学主管,同时也是James F. Jackson 和Luther Dana Waterman 双重名誉教授。
Flood教授课题组近期对溶液中阴离子识别的驱动机理做出了重要突破。这个突破不仅为溶液中主客体结合能预测提供重要实验和理论双重依据,更是为主体分子设计过程中溶剂效应的考量提供了基础。该成果以封面文章的形式发表在最新一期Chem 杂志上。

图3. Flood教授课题组的封面文章。图片来源:Chem
溶剂效应对于任何化学过程都十分重要。由于主客体依赖弱相互作用,这更是凸显了溶剂对最终结合效率和选择性的影响。传统上,这类研究依赖于线性自由能关系。如果溶液中结合自由能与溶剂的某个或某些个物化性质呈线性关系,那么该物化性质被认为参与影响了溶液中主客体的结合。对阴离子识别来说,溶剂受体数(Acceptor Number, AN)衡量了溶剂的亲电性并在传统上被广泛认为是描述溶液中阴离子识别的良好物化性质。可是事实上此类研究受限于主体分子的构象可随溶剂变化而变化,阴离子结合自由能测量过程中没有考虑所有存在的化学平衡,以及被研究溶剂物化性质范围有限等等。因此人们无法仅仅依赖AN对溶液中阴离子结合能进行准确的预测。
对Triazolophane的详细研究打破了以上局限。Flood课题组已发表了诸多文章表征了溶液中Triazolophane识别Cl–离子的所有化学平衡。同时Flood教授与同校的理论化学家Krishnan Raghavachari教授早已阐述了Triazolophane的完整构象分析。这些科研基础奠定了在任意溶剂中研究并定量Triazolophane•Cl–结合能的可靠性,并使理论-实验定量关联成为了可能。
与预期的AN简单关联相悖,Flood课题组发现排除一切干扰因素并在尽可能大的溶剂物化参数范围内进行测量之后,溶液中阴离子结合能在非质子溶剂中与溶剂介电常数的倒数(1/εr)呈现线性关系(图4);在质子溶剂中,在考虑介电常数之后,还与溶剂氢键给体酸性(α)有关。这后一种关联与Chris A. Hunter教授对中性分子间氢键作用的研究成果是一致的;可想而知,像水这样的氢键给体对阴离子可以更有效的溶剂化,减弱主客体结合能。但是前一种关联在中性主体分子中未见报道。
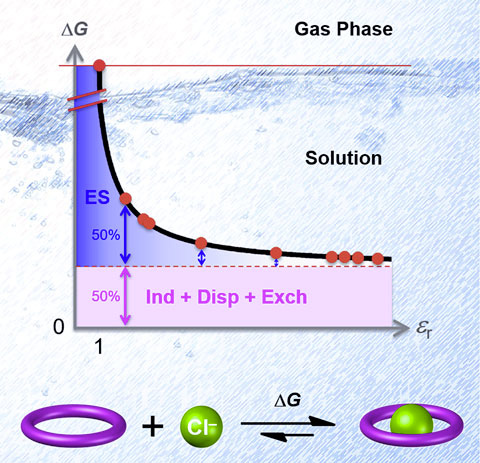
图4. 溶液中阴离子结合能的分解及其与溶剂介电常数的关系。图片来源:Chem
为了进一步阐明介电常数的影响,Flood教授与Raghavachari教授合作使用电子密度泛函理论(Density Functional Theory, DFT)配合内隐溶剂化模型尝试计算溶液中Triazolophane•Cl–的结合能。在5个纯溶剂中计算结果与实验几乎达到了1:1的线性关联(图5)。其中,内隐溶剂化模型将溶剂描述为一个连续介质,其物化性质主要由介电常数表征。
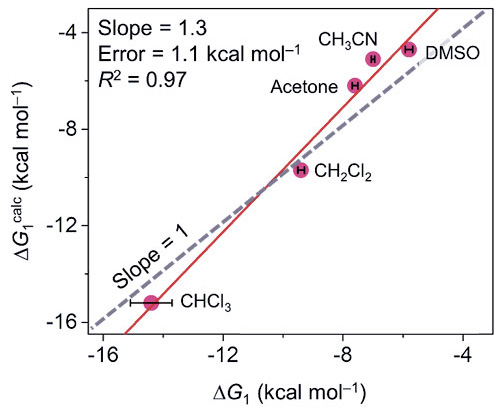
图5. 理论计算与实验测量的溶液中阴离子结合能呈线性相关。图片来源:Chem
计算与实验的1:1相关为简化溶剂效应提供了理论基础。文章通过几步公式推导,发现自由能中依赖于介电常数的部分可以由理论或者实验数据拟合而出(图6)。这部分能量即是阴离子与主体结合过程中静电相互作用产生的自由能。文章还将由连续介质假设下推导出的静电作用能与更为严格的对称性匹配微扰理论(Symmetry-Adapted Perturbation Theory, SAPT)计算出的静电作用能进行对比,发现二者高度相关:前者是结合能的76%,后者是82%。
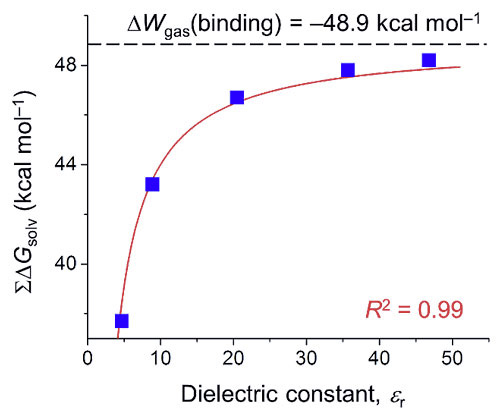
图6. Triazolophane•Cl–结合能中静电作用能的拟合。纵轴是去溶剂化能,横轴是介电常数。假设连续介质,静电作用能数值上等于无穷大介电常数时的去溶剂化能。图片来源:Chem
实验测定、量化计算与理论推导三者一致阐明了溶液中阴离子识别的驱动力分配。静电作用虽然主导了结合能,但是因为介电屏蔽其在实际溶液中的贡献随介电常数增大而越来越小。拿Triazolophane•Cl–举个例子,在非极性的氯仿中,静电作用的实际贡献已经降到了50%(图4)。其他作用,例如诱导,色散及排斥等短程作用在实际中的贡献与溶剂相对无关。要指出,因为Triazolophane几乎不带偶极矩,否则诱导作用也可与溶剂相关。
这些重要发现可以归纳在一个简单的关系式中(图7):溶液中阴离子结合能由气相结合能、静电作用能、介电常数、氢键给体溶剂的摩尔比和氢键给予强度决定。这个关系式不仅适用于之前表征过的溶剂,它还可以用于结合能的快速预测。文章中选用了1,2-二氯乙烷和硝基苯两种溶剂作为预测对象,因这二者在工业界液液萃取中被广泛应用。实验结果发现预测与实验值相比误差仅有0.6 kcal mol–1。
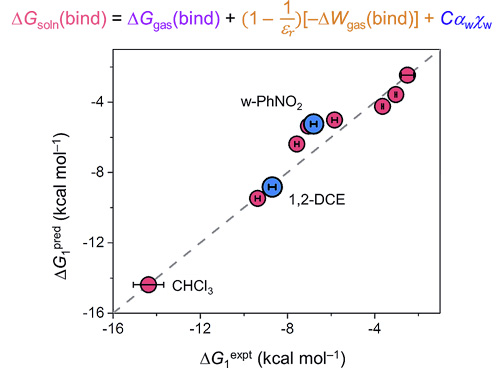
图7. Triazolophane•Cl–溶液中结合能的预测:红点表示公式拟合使用的7种溶剂,蓝点表示应用公式进行预测的两种溶剂。图片来源:Chem
笔者认为这项研究成果可以促使化学家在设计主体时引入溶剂效应。通过合理设计主体分子以改变其对客体结合时静电作用能的大小,人们可以调控溶液中结合能在不同溶剂中的大小。简单地说,人们可以通过减少结合能中静电作用的部分来增加极性溶剂中的结合能,而这又可以通过选用不同的弱相互作用得以实现。当然该文章还指出了进一步推广该研究成果必要的其他步骤,比如考虑柔性分子的构象,推广现有理论到其他混合溶剂,以及主客体不匹配时的情况。
在同期杂志上,爱丁堡大学化学院的Scott L. Cockroft教授为本文撰写评述(Chem, 2017, 3, 383),高度评价了该文章对溶液中阴离子识别机理研究的贡献。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Anion Binding in Solution: Beyond the Electrostatic Regime
Chem, 2017, 3, 411-427, DOI: 10.1016/j.chempr.2017.08.003
导师介绍
Amar H. Flood
http://www.x-mol.com/university/faculty/1167
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!




























 京公网安备 11010802027423号
京公网安备 11010802027423号