可见光氧化还原催化剂参与的1,7-烯炔串联环化反应合成稠环吡喃化合物
过渡金属催化的1,7-烯炔串联环化反应作为一种简单高效地构建C-C键的方法,一直是有机合成中的热门研究领域。酰基自由基是一种十分有用的自由基中间体,但由于自身的亲核性限制以及产生酰基自由基所需要的苛刻反应条件,在有机合成中的应用却远不及简单的烷基自由基甚至是烯基自由基频繁。基于以上情况,兰州大学功能有机分子化学国家重点实验室的许鹏飞教授(点击查看介绍)课题组报道了可见光氧化还原催化剂作用下芳基酰氯产生芳酰基自由基,与1,7-烯炔串联环化合成稠环吡喃结构的反应。

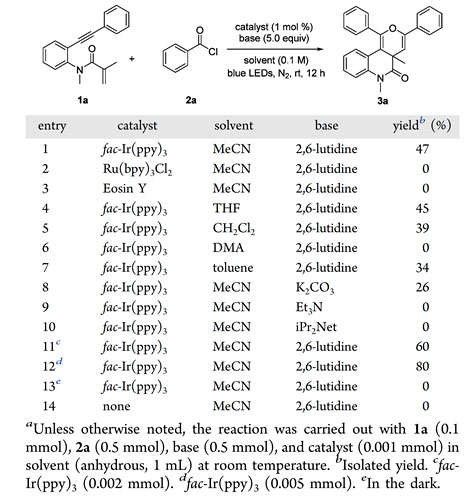
作者选择1,7-烯炔1a和苯甲酰氯2a作为底物进行条件筛选,当加入光催化剂fac-Ir(ppy)3和2,6-二甲基吡啶时,串联环化反应得以发生,以47%的产率得到预期产物3a (entry 1)。通过对反应条件的进一步优化,他们最终得到的最佳反应条件是:1,7-烯炔1a (0.1 mmol),苯甲酰氯2a (0.5 mmol)和光催化剂fac-Ir(ppy)3 (0.005 mmol)加入1 mL的乙腈体系,室温条件下氮气保护,以5 W蓝色LED灯照射12个小时,最终分离得到目标产物。同时,他们通过对照实验证明了光氧化还原催化剂以及可见光对反应发生的必要性。
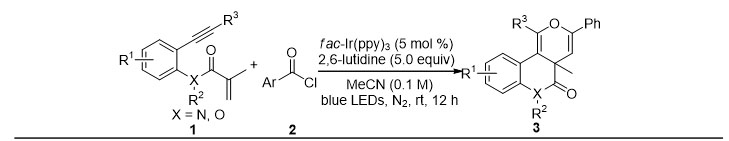
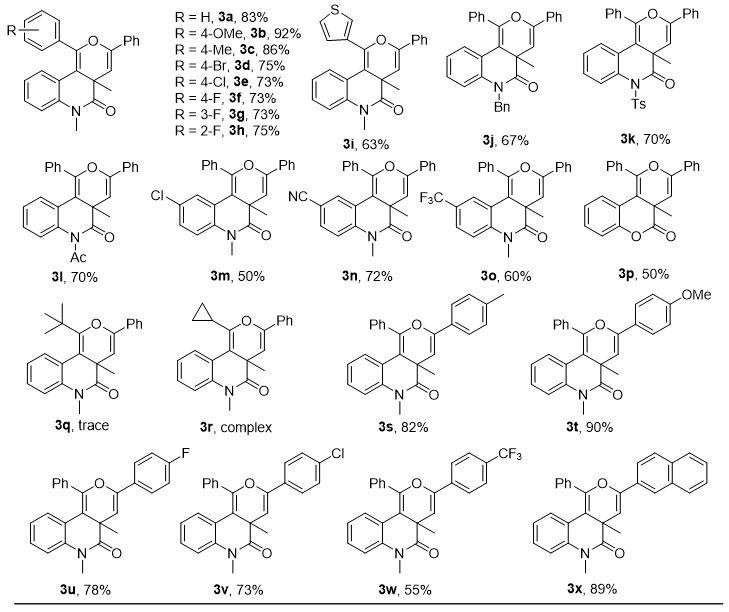
得到最优条件后,作者又对底物普适性进行了考察。他们首先固定苯甲酰氯2a,一系列的1,7-烯炔都能以较高的产率得到目标产物。分析结果发现,炔烃端位有富电子芳香环取代时产率明显高于缺电子芳香环(3a-3i)。内酰胺的氮上有不同取代基时,均能以良好的产率得到目标产物(3j-3l)。当氮原子相连的芳香环上有取代基时,反应依旧可以顺利发生(3m-3o)。将酰胺结构换成酯时,也能以较好的产率得到相应的产物,大大提高了底物的适用范围(3p)。但是,当炔烃端位有烷基取代时,反应无法进行或者得到的体系十分复杂(3q,3r)。随后作者还固定了1,7-烯炔1a,对不同取代的酰氯底物进行考察。从实验结果可以看出,富电子的芳基酰氯的反应产率普遍高于缺电子的芳基酰氯(3s-3x),这可能是因为富电子的芳香酰基不仅可以稳定反应中产生的正离子中间体,还有利于羰基氧对碳正离子的进攻。4-三氟甲基苯甲酰氯的反应活性较低,将反应延长到18小时仍然有部分1,7-烯炔未发生反应,只能以55%的产率得到目标产物。
作者为了验证反应机理,设计了荧光淬灭实验,并根据Stern-Volmer方程进行了线性拟合。结果显示,只有苯甲酰氯能够淬灭fac-Ir(ppy)3,而2,6-二甲基吡啶对fac-Ir(ppy)3没有影响,这就证明了反应确实是从苯甲酰氯开始启动的。同时,作者还向反应体系中加入了常用的自由基捕获剂四甲基哌啶氧化物(TEMPO),体系中的酰氯随之消失,但是并没有得到稠环吡喃化合物3a,只得到大量苯甲酰基取代的TEMPO化合物11,从侧面证实了反应中确实有苯甲酰基自由基产生。

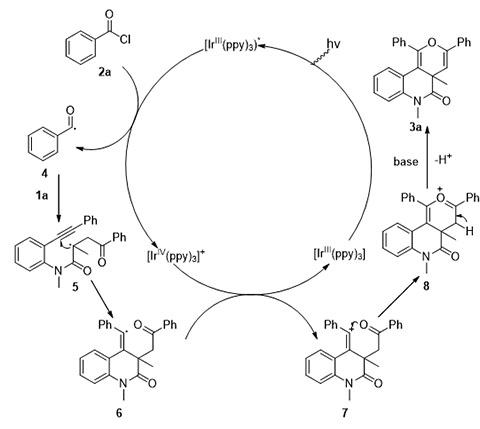
作者提出了可能的反应机理:光氧化还原催化剂通过单电子转移的方式还原芳基酰氯2a产生芳香酰基自由基4,随后芳香酰基自由基与1,7-烯炔1a发生串联反应,经自由基中间体5生成自由基中间体6,此中间体被高价态的光催化剂IrIV氧化,产生正离子中间体7,羰基上的氧进攻缺电子的碳位点产生氧鎓离子中间体8,并在碱的作用下失去质子得到目标产物3a。
总结
许鹏飞教授课题组发展了一种以芳基酰氯作为芳香酰基自由基前体,在可见光参与的条件下与1,7-烯炔发生串联反应,合成了一系列稠环吡喃类化合物。该反应条件温和,具有良好的底物普适性,同时也简化了反应的后处理方式。该策略还可以应用到其他杂环结构的合成中(Org. Chem. Front., 2017, DOI:10.1039/C7QO00012J)。这一成果近期发表在Organic Letters 上,文章的第一作者是兰州大学硕士研究生李晨光。
该论文作者为:Chen-Guang Li, Guo-Qiang Xu, and Peng-Fei Xu
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Synthesis of Fused Pyran Derivatives via Visible-Light-Induced Cascade Cyclization of 1,7-Enynes with Acyl Chlorides
Org. Lett., 2017, 19, 512-515, DOI: 10.1021/acs.orglett.6b03684
导师介绍
许鹏飞
http://www.x-mol.com/university/faculty/11187
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!



























 京公网安备 11010802027423号
京公网安备 11010802027423号