毒胡萝卜素的全合成:Evans vs. Baran,谁更高效?
毒胡萝卜素(Thapsigargin)是复杂的高氧化态倍半萜内酯,1978年由Christensen等人从地中海植物毒胡萝卜(Thapsia garganica)中分离得到,同时还分离出一大类愈创木内酯(guaianolide)结构的天然产物(图1),这些天然产物统称为thapsigargins。毒胡萝卜素是细胞内钙离子转运酶的高效抑制剂,选择性达到纳摩尔级别,该分子的C-8酯基衍生物Mipsagargin(G-202)作为前药目前已处于临床二期实验。
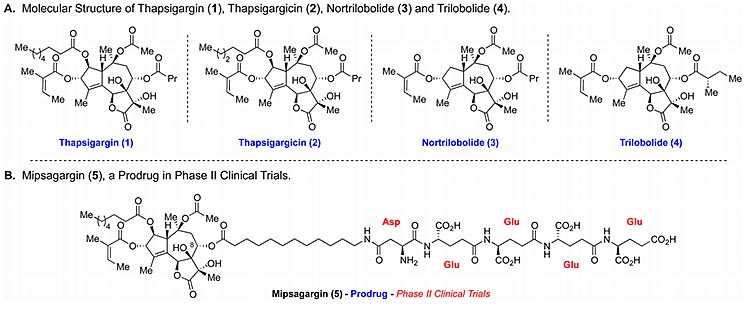
图1. 毒胡萝卜素及其类似物的结构。图片来源:JACS
毒胡萝卜素由于其独特的结构和潜在的生物活性,吸引了众多有机合成化学家对该分子进行合成研究,早些年的S. V. Ley(Org. Lett., 2007, 9, 663-666)以及近期的Phil S. Baran都报道过毒胡萝卜素的全合成(ACS Cent. Sci., 2017, 3, 47-51,点击阅读详细)。最近,加拿大女王大学化学系的P. Andrew Evans教授在JACS 上报道了该课题组对于毒胡萝卜素精彩的全合成,作者从手性原料香芹酮出发,总共12步完成了毒胡萝卜素简洁高效且可以大规模制备的全合成。论文第一作者为Evans组博士生Dezhi Chen。

P. Andrew Evans教授(左)和Dezhi Chen(右)。图片来源:Queen's University
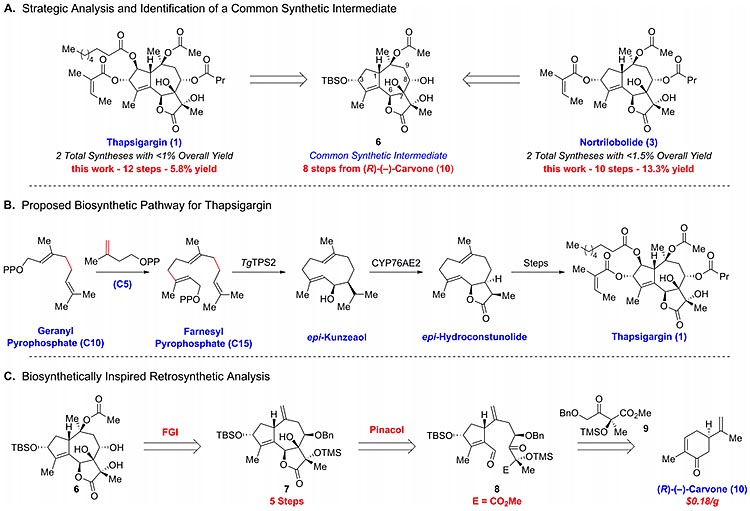
图2. 毒胡萝卜素的生源合成假说及本文的合成策略。图片来源:JACS
如图2所示,对于毒胡萝卜素及其类似物Nortrilobolide,都可以逆推至共同的关键中间体三环化合物6。而毒胡萝卜素的生源合成可能如图2B所示,5C单位的片段和10C单位的片段偶联之后,在环化酶的作用下关环得到epi-Kunzeaol,接着发生氧化内酯化,最后经数步转化得到目标分子。基于生源合成假说,作者提出的逆合成分析如图2C,关键中间体6可以由7制得,7则由化合物8发生醛酮的Pinacol偶联反应得到,8可以逆推至商品化的原料R-香芹酮,后者廉价易得,1克仅售18美分。
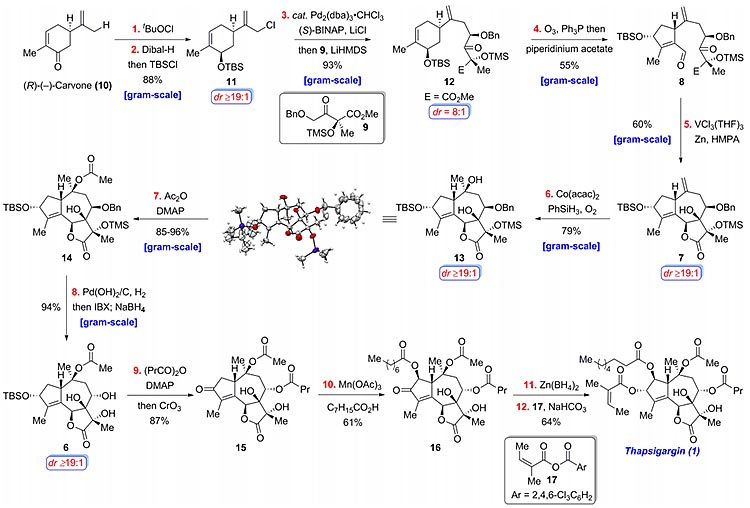
图3. 毒胡萝卜素的全合成。图片来源:JACS
具体合成过程如图3所示,作者从R-香芹酮出发,烯丙基位氯代、DIBAL-H还原酮羰基,随后羟基TBS保护得到化合物11。钯催化的氯代物和羰基α-位的交叉偶联反应得到化合物12,臭氧化选择性切断六元环上的双键并发生分子内缩合得到五元环的不饱和醛8,将8的溶液慢慢加入到[V2Cl3(THF)6]2[Zn2Cl6]溶液中,醛酮羰基还原偶联并发生原位内酯化得到内酯化合物7,d.r.选择性大于19:1,选择性Mukaiyama水合,在位阻较小的端烯处以优秀的d.r.选择性发生水合得到叔醇13,并由单晶确定了其结构和立体化学,乙酰基保护叔醇得到14,氢氧化钯条件下消除苄基保护基,IBX氧化后硼氢化钠还原得到羟基构型翻转的产物6,选择性依然十分理想,所有这些步骤都可以克级规模制备。作者还从6出发,先将二级醇羟基酯化,接着Jones氧化原位消除羟基的TBS保护基,并将其氧化为不饱和酮得到15,三价锰条件下在混合溶剂中羰基α-位氧化羟基化并发生原位酯化,以中等收率得到化合物16,最后,硼氢化锌还原酮羰基并与酸酐17发生Yamaguchi酯化,完成了毒胡萝卜素的全合成,整条合成路线非常简洁高效,并且可以实现大量制备。
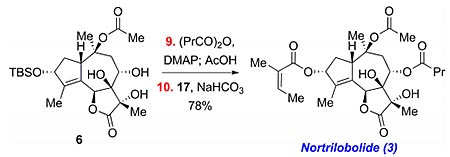
图4. Nortrilobolide的全合成。图片来源:JACS
作者继续从关键中间体6出发,先对8位的羟基进行酰化得到丁酯,在醋酸条件下原位消除五元环上羟基的TBS保护,最后再和酸酐17发生Yamaguchi酯化,就完成了另一个天然产物Nortrilobolide的全合成。
Baran的ACS Central Science 论文和Evans的JACS 论文发表前后仅相隔约四个月,与十年前的Ley的42步全合成路线相比都有很大的进步。对比之下,哪个小组效率更高呢?
Baran小组的11步合成路线,总产率0.137%,14步合成路线,总产率0.637%。而Evans小组从手性原料香芹酮出发,以Pinacol偶联/原位内酯化反应等关键步骤以12步完成了毒胡萝卜素的全合成,总产率5.8%,还可以大规模制备。同时,Evans小组还从关键中间体6出发,两步完成了另一个天然产物Nortrilobolide的全合成,总产率13.3%。另外,关键中间体7的合成是目前为止最简洁的合成愈创木内酯骨架的方法。
Evans的JACS文章也得到了C&EN的亮点评述[1],Christensen认为,P. Andrew Evans教授对于高度氧化的核心骨架的构建能在早期以正确的立体构型合成是至关重要的,这使得整体合成、对类似物的合成以及构效关系的研究更加方便。西班牙加迪斯大学(University of Cádiz)的Javier Moreno-Dorado说,P. Andrew Evans和Phil S Baran的合成路线哪个更高效还存在争议,很难去评判他们的效率高低。但这两条路线都使得毒胡萝卜素及其类似物的大规模合成成为可能,对于新药发现都具有重要意义。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

A Concise, Efficient and Scalable Total Synthesis of Thapsigargin and Nortrilobolide from (R)-(−)-Carvone
J. Am. Chem. Soc., 2017, 139, 6046−6049, DOI: 10.1021/jacs.7b01734
参考资料:
1. http://cen.acs.org/articles/95/i19/Improved-routes-thapsigargin.html
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!



























 京公网安备 11010802027423号
京公网安备 11010802027423号