细胞内高分辨DEER距离的测量
在细胞内研究蛋白质的结构、相互作用和动态变化对于了解生命过程具有重要意义,但细胞内高分辨研究蛋白质作用的细微机制通常需要借助于探针方法。近年来双电子自旋共振(double electron-electron resonance, DEER)技术成功应用于材料化学特别是生物大分子研究领域。该技术在大分子上的两个位点标记顺磁中心(通常是等同的顺磁中心),通过顺磁中心的偶极作用可以获得两个顺磁中心的距离信息,这与生物体系中通常用到的荧光能量共振转移(FRET)原理较为类似。DEER成为继FRET测定大分子距离信息的重要技术,顺磁探针的体积通常比荧光探针小,并且DEER测定的距离受其他因素的干扰少,因此DEER在生物体系中的应用最近才得到意识。DEER测定的距离分布宽窄决定着分辨率的高低,如何窄化测定的距离分布是目前DEER发展的一个重要方向。另外,细胞内的DEER测定与细胞外的研究需要克服探针的稳定性,通常DEER测量中用到的游离基在细胞内稳定性差,一些过渡金属离子探针的细胞毒性和与细胞内源金属蛋白的竞争也是一个挑战。
最近南开大学的苏循成(点击查看介绍)团队和以色列威兹曼科学研究院Daniella Goldfarb(点击查看介绍)教授合作发展了细胞内DEER测量的方法,并成功结合生物核磁和电子自旋共振方法研究细胞内蛋白质的动态行为。以色列威兹曼研究院Daniella Goldfarb教授提出了通过Gd(III)-Gd(III)测定大分子距离,在高场状态下,Gd(III)给出非常窄的-1/2到1/2的跃迁峰,并成功应用到大分子距离测量中(Phys Chem Chem Phys, 2014, 16, 9685-9699)。南开大学的苏循成课题组自2013年起与Goldfarb教授在发展顺磁探针并利用NMR和EPR技术研究蛋白质结构和动态学方面展开了积极合作。最近两个课题组发展了通过核磁共振优化顺磁探针的刚性,并成功应用于DEER距离的测量,展示了顺磁核磁共振中PCS和RDC的综合利用,不但可以揭示蛋白质的动态变化,还可以通过顺磁核磁发展的刚性顺磁探针窄化DEER测定的距离分布(Dalton, 2015, 44, 20812-20816)。继PCS成功测定活性细胞内蛋白质的三维结构(Chem. Commun., 2016, 52, 10237-10240)的基础上,中方课题组通过生物核磁共振技术发展了一类高活性的大环探针,这类探针与蛋白质定点反应的活性高并且专一性好(图1)。

图1. 应用于细胞内DEER距离测量的蛋白质定点标记路线。
该类大环探针定点标记的蛋白质在高分辨核磁共振波谱中表现出良好的刚性和稳定性(图2),磁各向异性的镧系离子标记后的蛋白质在核磁共振波谱中产生显著的PCS,并由于吡啶氮的配位极大增强了探针的刚性。
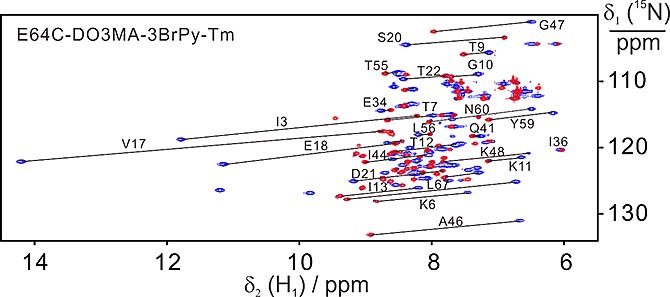
图2. DOTA大环探针定点标记ubiquitin E64C的异核单量子相关谱(15N-HSQC),其中DO3MA-3BrPy-Tm标记的蛋白(蓝色),DO3MA-3BrPy-Y(红色)。
通过核磁共振优化的DO3MA探针同时应用于蛋白质的双标记。以ubiquitin E64C/G35C、E64C/D39C和E64C/L73C三对双突变体为目标蛋白,DO3MA-3BrPy-Ln标记的反应在室温和pH=8的条件下6个小时内完成,标记效率达到80%。中方课题组通过核磁共振技术发现引入顺磁探针后对蛋白质结构的影响很小,并且顺磁探针在两个位点的磁感应张量Δχ 可以叠加,充分说明修饰到蛋白质上的两个顺磁中心的刚性。随后以色列课题组对标记的蛋白质进行了细胞外和细胞内的DEER测定,并且对把蛋白质导入细胞的不同方式行了比较(图3和图4)。
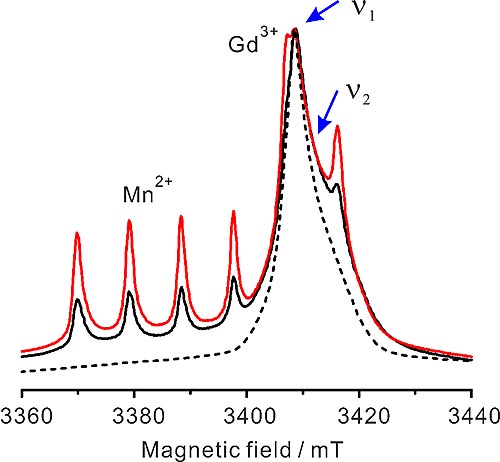
图3. 10 K下W-波段的ED-EPR谱。图中可以看出细胞内源的Mn2+具有较高的浓度,其中红色和黑色分别是把目标蛋白以低渗透和电转方式导入细胞中的图谱。

图4. W-波段的DEER谱,其中A和C中分别以低渗透和电转方式把标记的目标蛋白导入到活细胞后不同培养时间段的EPR谱;B和D分别是A和C数据拟合得到的距离信息。
研究人员对导入细胞后顺磁标记的蛋白质在细胞培养里进行了稳定性跟踪,并通过不同培养时间段的细胞分别进行了EPR测定(图4)。这类刚性的顺磁探针给出了预期的窄距离DEER测量结果,结果表明DO3MA-3BrPy-Gd探针在细胞内具有较高的稳定性,在活细胞内能稳定10小时以上,并且没有发现多聚泛素化的发生。由于ubiquitin在细胞内难以观察到核磁信号,而DEER的结果充分表明顺磁核磁和电子顺磁共振在研究细胞内大分子作用、结构和动态变化过程的高度互补性。这一成果近期发表在Angew. Chem. Int. Ed. 上。
该论文作者为:Yang Y, Yang F, Gong YJ, Chen JL, Goldfarb D, Su XC.
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

A reactive, rigid GdIII labeling tag for in-cell EPR distance measurements in proteins
Angew. Chem. Int. Ed., 2017, 56, 2914-2918, DOI: 10.1002/anie.201611051
导师介绍
苏循成
http://www.x-mol.com/university/faculty/11898
Daniella Goldfarb
http://www.x-mol.com/university/faculty/40466
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!


























 京公网安备 11010802027423号
京公网安备 11010802027423号