在人类与病菌的战争中,谁能笑到最后?
几个月前,美国发现第一个被携带mcr-1基因的大肠杆菌感染的病例,再次拉响了对病菌抗生素耐药性的警报。再早些时候,中国的科学家发现了使得细菌获得粘菌素(colistin)耐药性的基因,欧洲和加拿大也相继出现了耐粘菌素细菌。尽管粘菌素在上世纪七十年代因毒性太大失宠,它却是人类抵抗耐多药细菌感染的最后一道防线,现在它也面临被攻破的风险。
根据美国疾病控制与预防中心(CDC)的统计,耐药性病菌已经在美国造成每年至少两百万人患病和23000人死亡,在欧洲造成类似规模的危害。其中艰难梭菌(Clostridium difficile),耐碳青霉烯肠杆菌(carbapenem-resistant Enterobacteriaceae)和耐药性淋球菌(Neisseria gonorrhoeae)是三个最大的威胁。其次是ESKAPE组合,即耐药性的粪肠球菌(Enterococcus faecium)、金黄色葡萄球菌(Staphylococcus aureus)、肺炎克雷伯菌(Klebsiella pneumoniae)、鲍曼不动杆菌(Acinetobacter baumannii)、绿脓杆菌(Pseudomonas aeruginosa)、肠杆菌(Enterobacter)。
尽管耐药菌的威胁已经愈来愈严重,但现在人类的药物武库中仅有40种小分子和24种其他治疗方案(如抗体、疫苗)在进行临床测试,但能成功熬过临床试验最终获批的仅仅只有五分之一。现在处于三期临床阶段的抗生素如下图所示:

进行三期临床试验的抗生素。数据来源:Pew Charitable Trusts as of May 2016, company information
抗生素研究在上世纪五十年代达到全盛时期,但随着研发出的新药逐渐渐少,收益预期缩水,抗生素研发呈现萎缩的状态,除了几家大型制药公司外,其他公司几乎全部撤出。尽管现在有一些小公司重新捡起了这项工作,但是抗生素研发依然是场艰苦的持久战,要想赢得胜利,需要科学、管理和财力的齐心协力。
2000年以来,新类型的抗生素屈指可数。追踪抗生素研发的Pew Charitable Trusts指出,过去30年几乎所有获批的抗生素都是已有药物的改良版。人们担心,当这一类的药物中的一个失效时,同类的其他药物也将在耐药菌面前迅速溃败。
前默克科学家Lynn Silver说,“我们要搞明白怎样才能把抗生素化学做的更好”。她很希望看到更多能够杀死革兰氏阴性菌的化合物,大部分难对付的耐药菌(如ESKAPE和三大威胁)都是革兰氏阴性菌。这类细菌的外层细胞膜结构很复杂,药物想要通过从而进入细菌内部变得更加困难。“我们没有理想的方法来解决这个问题,这阻碍了我们继续前行。”她还补充到,“现在抗生素研究大部分是对老药的修饰,使它们能够更强效,能够对抗耐药菌。”
不过,这是一场和时间的赛跑,因为抗药性可能因某个小变异而一夜之间就产生,Silver解释说。现在好的抗生素应针对多个靶标,或者具有不会引起抗性的其他特征。
细菌的耐药性已经消弱了四环素类抗生素的效果,这种有70年历史的广谱抗生素,曾是抗感染的重要药物。Paratek Pharmaceuticals是活跃在抗生素研发领域的小公司之一,他们试图改造四环素类。通过构效关系改变米诺环素母核上的取代基,试图避开两种最常见的抗性机理。其中一种方式是避免被外排泵识别,细菌通过外排泵捕获抗生素并将其排出体外;另一种方式是阻止细菌对它们核糖体上一些关键位点的保护,很多类型药物包括四环素类都是结合在这些位点上并抑制细菌蛋白质合成。这个成立20年的公司拥有口服和静脉注射剂型的omadacycline(一种氨甲环素),现在进入到三期临床。Omadacycline对革兰氏阴性菌有效,但一开始测试的重点是治疗细菌性肺炎和皮肤感染(往往由革兰氏阳性菌引起)。目前为止,Paratek还未看到omadacycline有引起抗性的迹象,但别忘了细菌产生抗性的能力和速度。如果使用不当导致抗性的确产生了,Paratek预计病菌对omadacycline产生抗性所需要的时间要比其他种类的抗生素(如喹诺酮类)多一些,这样一来,omadacycline就有望取代它们。Omadacycline也有望成为2005年以来获批的第一个四环素类广谱抗生素。
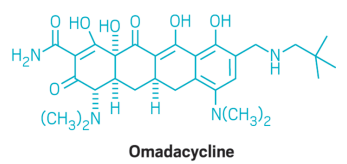
图片来源:C&EN
2012年美国抗生素激励法案Generating Antibiotic Incentives Now Act颁布,美国FDA也随即更新了他们的政策,并发出了新的指导原则。FDA同时开始向治疗严重或危及生命感染的药物颁发“合格传染病产品(QIDP)”认证。获得QIDP认证的药物享有加急审批的待遇,同时在专利到期之后还享有额外5年的市场独占权。因为各种问题Paratek的omadacycline项目曾一度停摆,但拿到QIDP认证之后,这些政策红利帮助Paratek重启了omadacycline项目。
与Paratek类似,另一家成立10年的公司Tetraphase Pharmaceuticals也在开发四环素类似物。现在公司有2000多个潜在的药物,不同于半合成,它们全部是一步步合成出来的,每步都试图避免已知抗性机理。其拳头产品、同样获得QIDP认证的eravacycline在三期临床试验中表现喜忧参半,在治疗复杂性腹腔内感染(cIAIs)的临床试验中非常成功,但在治疗复杂性尿路感染(cUTIs)未能达到终点目标,而这两种病往往都是由革兰氏阴性菌引起。尽管eravacycline口服制剂表现不佳,Tetraphase仍专注于开发口服处方,因为目前很少有口服抗生素能够对抗耐多药的革兰氏阴性菌感染。除此之外,Tetraphase还有两个药处于开发初期阶段,TP-271用于呼吸系统感染,TP-6076用于抗碳青霉烯耐药菌。

图片来源:C&EN
Cempra也对已知抗生素进行化学修饰,制造新分子结构,例如改变大环内酯类的化学结构,使其与细菌核糖体的结合位点从1个增加到3个。现在有25%的肺炎病例都对大环内酯类抗生素有耐药性,Cempra的solithromycin能在治疗开始的前3天中就让约80%的患者产生响应,这和常用的莫西沙星效果相当。
还有家小公司,Melinta Therapeutics正翘首以盼Baxdela(delafloxacin)的获批,delafloxacin的口服和静脉注射剂型,可以治疗耐甲氧西林菌金黄色葡萄球菌(Staphylococcus aureus)引起的医院获得性肺炎和皮肤感染。Baxdela是氟喹诺酮类药物,但与其他同类化合物的大小和价态不同,而且更强效,抗性难以发生。Melinta还有三款基于结构设计的药物,希望其中之一的pyrrolocytosine能在2017年开展临床试验。

图片来源:C&EN
Entasis Therapeutics是2015年从AstraZeneca拆分出的公司,他们的目标也是革兰氏阴性病菌。Entasis最先进的药物ETX0914(zoliflodacin)已经完成了二期临床试验,这种口服新型螺嘧啶三酮类化合物,用于治疗单纯性淋病。不同于氟喹诺酮类药物,它结合在药物靶标DNA促旋酶的新位点上。
Entasis也研究曾经广泛使用的β内酰胺类抗生素,试图使其重获新生。耐药菌进化出β内酰胺酶来分解这类药物,相应的解决策略是同时使用β-内酰胺酶抑制剂,但抗性的发展很快,因为这些抑制剂有时候本身就是β内酰胺类。2015年FDA批准了AstraZeneca和Allergan的Avycaz,就含有非β内酰胺结构的β内酰胺酶抑制剂avibactam和第三代头孢ceftazidime。Merck的新抑制剂relebactam也在三期临床中,Medicines Co.也正研究一种含硼的抑制剂。Entasis的候选药物ETX2514是一种diazabicyclooctenone类β内酰胺酶抑制剂,能抑制多种β内酰胺酶,因此可以扩大β内酰胺类抗生素的抗菌谱。
对抗革兰氏阴性菌的另外一种策略是使用抗革兰氏阳性菌药物。“对革兰氏阴性菌来说,不可能遇到过抗阳性菌的药物,也就不会产生抗性”,Spero Therapeutics的CEO Ankit Mahadevia说到。革兰氏阴性菌的细胞壁犹如坚硬外墙,要用这种策略杀死病菌,需要先解决细胞壁的问题。Spero开发增效剂来和细胞壁中的脂多糖相互作用,增加细胞壁通透性,以此来瓦解细胞壁的保护。Spero公司正在测试增效剂与抗生素的联用效果,一项动物实验发现,单独用clarithromycin不但无杀菌效果反而细菌会增殖至少10倍,而联合SPR741用药则能让细菌减少100倍。第一个增效剂多粘菌素B衍生物SPR741的临床试验有望于近期举行。

SPR741与clarithromycin联合用药。图片来源:Nature Medicine
单克隆抗体(单抗)也能增强抗生素的效果,不过其机理却完全不同。Arsanis的目标更有野心,降低抗体药物对抗生素的依赖。该公司的单抗ASN100能中和能致病的细菌毒素,正进入二期临床试验。一剂ASN100包含两种不同的抗体,能阻止病菌产生毒性及导致肺炎。当毒素被中和后,机体能够清除病菌。因为抗体药物对付的是内毒素,而不是病菌本身,从而不会引起抗性。Arsanis也开发能够直接杀灭细菌的抗体药物,例如ASN-4,这种抗体的靶标是某些耐药大肠杆菌上的一种新受体。

小分子之外对付细菌感染的手段。数据来源:Pew Charitable Trusts as of May 2016, company information
还有一家小公司Achaogen,将抗体和小分子化合物组合起来抗革兰氏阴性菌。其中氨基糖苷类衍生物plazomicin,设计用来克服耐药菌对这类老抗生素的抗性。现在正进行两个三期临床试验,一是治疗cUTIs,一是治疗耐碳青霉烯肠杆菌引起的严重感染。

图片来源:C&EN
随着抗生素面临着的紧迫局面,一系列利好政策也陆续颁布。除此之外还有投资基金投入近来,过去10年,单美国政府就投资了10亿美元在抗生素研发上,还有各大小公司之间的项目收购,财力大大支持了抗生素的研发。另外,教育公众合理使用抗生素也非常重要,毕竟,人体内还要大量的有益微生物,人类和微生物间的和谐共处或许是这场旷日持久战争的终极解决方案。
文章编译自:
[1] Antibiotics: Will the bugs always win?
http://cen.acs.org/articles/94/i35/Antibiotics-bugs-always-win.html
[2] What's old is new: Reconfiguring known antibiotics to fight drug resistance.
Nature Medicine, 2016, 22, 1197-1199, DOI: 10.1038/nm1116-1197
