模块化生物催化不对称合成手性化合物
注:文末有研究团队简介及本文科研思路分析
通过一锅法实现多步串联催化反应是有机合成中的热点,它避免了传统的多步反应对中间产物的分离和提纯操作,既减少了有机废弃物的污染,又获得了更高的最终产率,同时还节省了人力、物力和时间的投入,从而提高了整体反应路线的经济性。从宏观和应用角度来看,倘若串联催化反应能实现同时进行且反应中间产物基本没有积累,这样的多步反应和单步反应是一样的,可以实现形式上新的化学反应类型。一锅串联反应的关键是多步反应的介质和条件要相似。相较化学催化反应(均相催化、非均相催化)多是在不同的条件下进行的,绝大多数酶催化的各类反应都是在相似的温和条件下(常压常温中性水溶液)进行的,例如生物体内的大部分酶都在细胞质中起作用。结合这一显著优点,可将多个酶合理组合通过一锅法来实现多步催化有用的反应,例如不对称合成手性化合物。
近日新加坡国立大学的LI Zhi课题组利用串联生物催化实现了三类不同的烯烃官能团化反应,从末端烯烃出发通过一锅法生成手性α-羟基酸、邻氨醇和α-氨基酸。基于生物催化的逆合成分析法,他们设计了三条从末端烯烃出发的酶催化路线。同时巧妙的结合了工程学和合成生物学的模块化思想,将两个主反应(及辅助反应)组合成一个酶催化模块,一共设计了四个酶催化模块,通过不同的模块间的自由组合来选择最优方案以实现这三类烯烃官能团化反应。
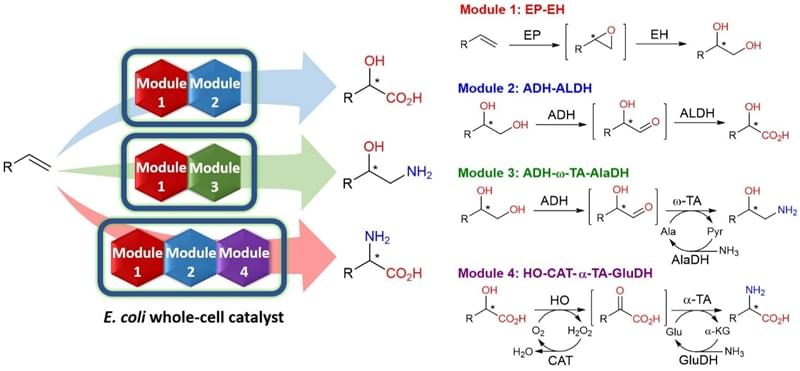
接下来他们以苯乙烯为底物生产手性扁桃酸、苯乙氨醇、苯甘氨酸作为模式反应。从多种微生物中,他们筛选并克隆了单加氧酶、还氧化物水解酶、醇脱氢酶、醛脱氢酶、ω-转氨酶、丙氨酸脱氢酶、羟基酸氧化酶、α-转氨酶、过氧化氢酶、谷氨酸脱氢酶。每一个模块中酶的基因序列全部克隆到一起,并分别构建到四个兼容的质粒上。通过将含有不同模块的质粒共同转入大肠杆菌,从而获得了一系列的大肠杆菌,每一株菌都可以同时表达4-8种酶。从这些菌株中,他们选出了三株最优的菌株来分别催化三类反应。利用一株菌,从11种(取代)苯乙烯,高转化率地生成11种(取代)(S)-扁桃酸,ee值达96-99%;利用另一株菌,可以反应生成11种(取代)(S)-苯乙氨醇,ee值达91-99%;还有一株菌,可以反应生成11种(取代)(S)-苯甘氨酸,ee值全部99%。上述反应还进一步放大到100mL在摇瓶中进行测试,成功制备了200mg-1g 的几种(S)-扁桃酸、(S)-苯乙氨醇和(S)-苯甘氨酸。

从简单易得的烯烃直接一锅法生成手性α-羟基酸和α-氨基酸在传统有机合成中尚未报道,而从生物催化法从烯烃生成手性邻氨醇(形式上的不对称氨羟基化反应),比著名的Sharpless不对称氨羟基化有更高的位置选择性和立体选择性。这三种生物催化烯烃官能团化反应全部在温和的条件下进行,并且只用便宜和绿色的葡萄糖、氧气和氨作为计量的反应物。
上述的三类反应是以烯烃作为底物的,工业上烯烃大都是从不可再生的化石燃料获得的,而绝大部分的不对称合成也是基于化石燃料作为底物。如果能直接从可再生的原料生成非天然的手性化合物,那将是非常有意思并且有前景的。很多天然氨基酸都是以葡萄糖等可再生原料通过微生物发酵来生产的。基于这一点,LI Zhi课题组设计了一个新的酶催化模块,并且和上一个项目的几个酶催化模块进一步组合,直接从苯丙氨酸一锅法生成非天然手性还氧化物、邻二醇、α-羟基酸和α-氨基酸。

首先,他们设计了一个由裂解酶和脱羧酶组成的酶催化模块来实现从苯丙氨酸生产苯乙烯,经过筛选和克隆,选取了来自植物拟南芥的最优裂解酶和来自黑曲霉的最优脱羧酶来实现这一反应。将这两个酶的基因构建到一个质粒上,经检测含有该质粒的大肠杆菌能高效转化苯丙氨酸生成14g/L的苯乙烯,转化率达92%。接下来,将该酶催化模块和单加氧酶模块组合转入大肠杆菌,得到一株最优的菌株来高效转化苯丙氨酸生成15g/L的(S)-苯乙烯环氧化物,转化率达89%,ee值99%。类似的,将裂解-脱羧酶模块和其它酶模块组合,得到一系列的大肠杆菌菌株,每一株菌都可以同时表达4-10个酶。其中最优的四株菌可高效转化苯丙氨酸分别生成(R)-苯乙二醇、(S)-苯乙二醇、(S)-扁桃酸和(S)-苯甘氨酸,转化率达85-91%,ee值96-99%。这些一锅反应均放大到100mL体系中,在摇瓶中从苯丙氨酸出发成功制备了300mg-1g的这些非天然的手性化合物。值得一提的是,因为大肠杆菌本身就有从葡萄糖合成苯丙氨酸的代谢途径,所以在上述大肠杆菌菌株培养过程中,对应的非天然的手性化合物已经在以葡萄糖为碳源的培养基中生成。虽然浓度不高,约100mg/L,但是它证明了从葡萄糖直接发酵生成一系列非天然的手性化合物的可能性。
这两项近期的成果展示了串联生物催化在不对称合成中的应用前景,并且为其它的串联催化提供了借鉴意义。随着生物技术领域的快速发展(合成基因、遗传改造、基因组改造、蛋白质定向进化等),生物法(酶催化、代谢工程、合成生物学)也将逐渐成为生产很多天然或人造的大宗化学品和精细化学品的重要方法。
上述研究成果分别在Nature Communications和Angew. Chem. Int. Ed. 上发表。
1.该论文作者为:Shuke Wu, Yi Zhou, Tianwen Wang, Heng-Phon Too, Daniel I. C. Wang, Zhi Li
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Highly Regio- and Enantioselective Multiple Oxy- and Amino-functionalizations of Alkenes by Modular Cascade Biocatalysis
Nat. Commun., 2016, 7, 11917, DOI: 10.1038/ncomms11917
2. 该论文作者为:Yi Zhou, Shuke Wu, Zhi Li
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Cascade Biocatalysis for Sustainable Asymmetric Synthesis: from Biobased ʟ-Phenylalanine to High-value Chiral Chemicals
Angew. Chem. Int. Ed., 2016, 55, 11647-11650, DOI: 10.1002/anie.201606235
LI Zhi教授简介

LI Zhi,新加坡国立大学教授
PhD (Org. Chem.) 维也纳大学, 1991
MEng (Chem. Eng.) 中科院, 1985
BSc (Chem.) 南京大学, 1982
研究领域主要是生物催化/酶催化,包括挖掘新酶、酶的定向进化、酶固定化、串联生物催化、新型生物材料以及代谢工程/合成生物学。2017年中会有1-3个博士后位置,欢迎有相关背景的同学加入我们团队。
实验室主页:
http://cheed.nus.edu.sg/stf/chelz/index.html
科研思路分析
Q:这项研究的最初目的是什么?或者说想法是怎么产生的?
A:我们课题组一直都在做生物催化方向的工作。早在2003年我们就发现了一些细菌内的烯烃还氧化-水解串联反应 (J. Org. Chem., 2003, 68, 8599)。后来把这个还氧化-水解串联反应(即形式上的不对称反式双羟化)继续深入做了不同底物,不同选择性,提高催化效率生成很多手性二醇(Chem. Commun., 2009, 1481; Green Chem., 2011, 13, 2452; ACS Catal., 2014, 4, 409)。后来就想利用串联生物催化做新的反应,直接生产更有用的高附加值的手性化合物。
Q:在研究中过程中遇到的最大挑战在哪里?
A:本项研究中最大的挑战是从各种生物中找到所有这些高效的酶。因为反应路线是人工设计的,很多时候并没有现成的已知酶可以用,而很多酶有较高的底物专一性。在这个过程中,我们团队在降解各种碳源的微生物方面的经验和积累起了重要的作用。此外,这项研究属于交叉学科的研究,虽然做的是不对称合成,其中需要不少基因工程来改造大肠杆菌,使其共同表达多达10个不同来源的酶,并且能调节其表达强度。而项目开始时,刚好有生物背景的学生加入我们团队,从而能在单个重组菌株内实现高效的3-8步串联催化。
Q:本项研究成果最有可能的重要应用有哪些?哪些领域的企业或研究机构最有可能从本项成果中获得帮助?
A:本项研究主要是用于生产几类手性化合物,例如手性α-羟基酸,邻氨醇,和α-氨基酸等等。其中,手性扁桃酸和苯甘氨酸都是非常重要的中间体,广泛用于生产手性药物和不对称合成等等。我们现在正在进行后续研究,提高反应效率和最终产物浓度,并且放大反应到发酵罐中,进一步降低生产成本和环境污染。欢迎国内的制药厂或精细化工厂联系我们洽谈合作事宜。并且我们组还有几种高效生产生物柴油的技术,也欢迎生物柴油厂家的合作。
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!



























 京公网安备 11010802027423号
京公网安备 11010802027423号