Angew:铜催化亚胺、联烯和硼试剂的多组分不对称加成反应
高烯丙基胺类化合物是一类非常重要的合成子,广泛地应用于药物、天然产物、催化剂以及配体的合成中。人们通常使用烯丙基金属试剂与亚胺进行不对称加成反应制备该类化合物,该方法可以高效的构建含一个手性中心的高烯丙基胺类化合物,而构建含两个手性中心的该类化合物存在诸多挑战,主要有以下几个原因:反应活性低,异构体难于调控,并可能存在E/Z选择性等(Scheme 1A)。另外,通过烯烃与硼试剂反应得到亲核性的中间体,进而与醛和酮反应的报道非常多,而与亚胺反应进而制备高烯丙基胺类化合物的报道还非常少,可能是因为亚胺的活性较低。Morken小组曾经使用钯催化剂,联烯、硼试剂和亚胺的多组分不对称加成反应,但也没能构建含两个手性中心该类化合物(Scheme 1B, J. Am. Chem. Soc., 2006, 128, 74),Morken教授的工作可能是唯一不对称的例子(Scheme 1B)。
最近英国曼彻斯特大学的David J. Procter教授报道了铜催化亚胺、联烯和硼试剂的多组分不对称加成反应,可以构建含两个手性中心的高烯丙基胺类化合物。(Enantioselective Generation of Adjacent Stereocenters in a Copper-Catalyzed Three-Component Coupling of Imines, Allenes, and Diboranes. Angew. Chem. Int. Ed., 2016, DOI: 10.1002/anie.201606710)

Scheme 1. 图片来源:Angew. Chem. Int. Ed.
Procter教授在之前发表了类似催化体系制备消旋高烯丙基胺类化合物的方法(Angew. Chem. Int. Ed., 2016, 55, 1102)。在此工作基础上,使用手性NHC*首次实现了该类反应的不对称加成。研究小组使用联烯2a和双硼试剂,在CuI作用下,对亚胺底物1a进行加成反应。主要考察了不同的手性卡宾配体,当使用商品化的手性卡宾前体4时没能得到产物,而使用卡宾前体5时能够以优秀的产率和选择性得到产物,将5换为6时能得到最好的结果(Scheme 2)。随后在最优条件下下对底物进行了拓展,其中亚胺底物1a上邻甲基苯基换为不同芳基,而且氮上也可以换为不同取代基,都能得到很好地结果。不同的单取代联烯底物也能很好地适用于该反应体系。
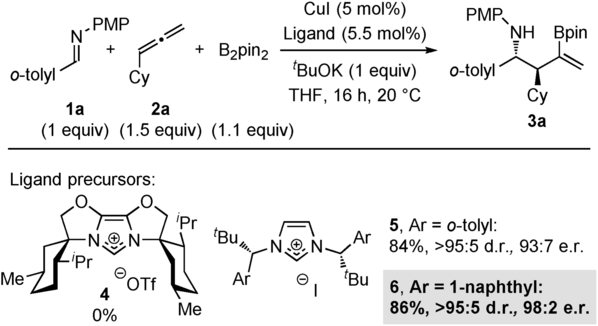
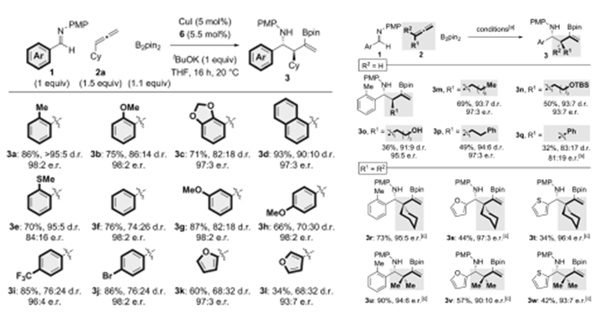
Scheme 2. 图片来源:Angew. Chem. Int. Ed.
研究小组对反应过渡态进行了推测,首先认为反应经过以下历程:在碱作用下先得到Cu-B中间体II,该中间体对联烯进行加成得到烯丙基铜中间体III,随后烯丙基铜对亚胺进行不对称加成,并最终脱除铜得到产物(Scheme 3)。基于此,在得到产物3w的单晶并确定产物绝对构型为R以后,研究小组推断出反应可能经过的六元环过渡态。
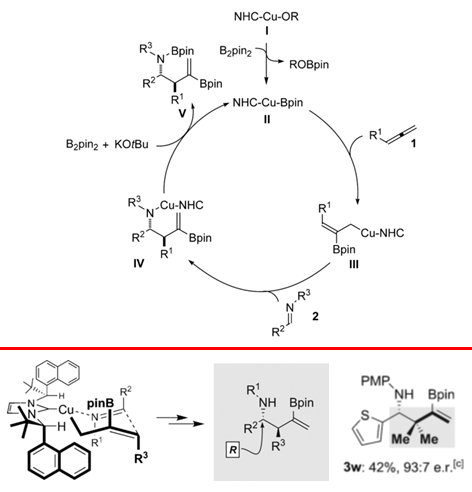
Scheme 3. 图片来源:Angew. Chem. Int. Ed.
最后,研究了该反应体系的应用前景。反应放大到克级规模也能够得到非常优秀的结果。产物在H2O2/NaOH作用下能够被顺利地氧化为酮7;在Pd/C作用下进行氢化反应,能够以54%的收率得到含有三个手性中心的产物8(Scheme 4)。
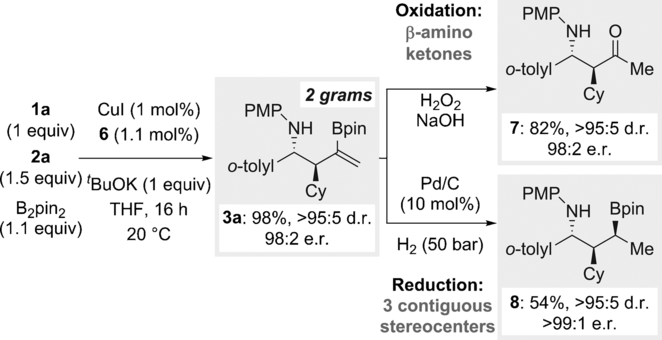
Scheme 4. 图片来源:Angew. Chem. Int. Ed.
总结:
Procter教授首次报道了高区域、高对映选择性地制备含两个手性中心的高烯丙基胺类化合物的方法。反应使用商品化的Cu(I)盐和NHC*配体,从简单的亚胺、联烯和双硼试剂出发,简单高效地得到产物,在合成中有着广阔的应用前景。
http://onlinelibrary.wiley.com/doi/10.1002/anie.201606710/abstract
David J. Procter 教授网站:http://people.man.ac.uk/~mbdssdp2/
(本文由moonlight供稿)
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!




























 京公网安备 11010802027423号
京公网安备 11010802027423号