新型茚并吡唑类微管蛋白抑制剂的设计与抗肿瘤活性研究
微管蛋白是抗肿瘤药物研究的有效靶点之一,以紫杉醇为代表的微管蛋白抑制剂是临床最有效的抗肿瘤药物之一。紫杉醇、埃坡霉素等作用于紫杉醇结合位点,能够抑制微管蛋白的解聚,使微管结构稳定;而长春碱和秋水仙碱则通过各自的作用位点,抑制微管蛋白的聚合。目前的临床药物紫杉醇、埃坡霉素等,因易产生获得性耐药性导致疗效降低,限制了它们的进一步应用。靶向秋水仙碱结合位点的小分子微管蛋白抑制剂一般不是多药耐药外排泵的底物,可以克服由P-糖蛋白介导的耐药机制,对多药耐药肿瘤细胞、紫杉醇耐药细胞依然有效,近年来倍受注目。
山东大学刘兆鹏教授课题组以秋水仙碱结合位点为靶点,基于微管蛋白秋水仙碱结合位点的晶体结构和计算机辅助药物设计和虚拟筛选与评价结果,设计合成了新型茚并吡唑类小分子微管蛋白抑制剂。通过初步抗肿瘤药理学筛选与评价,发现了两个具有极高活性化合物6a(LL01)和6n(LL02)。LL01竞争性作用于秋水仙碱结合位点,抑制微管蛋白的聚合,其活性与秋水仙碱相当;LL01和LL02对多种肿瘤细胞具有强抑制作用,IC50分别在7.1 ~ 32.3 nM和8.3 ~ 33.6 nM之间,优于紫杉醇或与紫杉醇相当。作为抗有丝分裂剂,LL01通过改变cyclin B1和p-cdc2的表达,使A549细胞分裂停滞于G2/M期;LL01通过激活相关凋亡蛋白caspase-3 和 PARP,诱导A549细胞。LL01还呈浓度依赖性地抑制人脐静脉内皮细胞毛细血管生成,预示其具有破坏肿瘤新生血管的潜力。在非小细胞肺癌裸鼠模型实验中,LL01具有良好的体内抗肿瘤活性,而未表现出明显的毒副作用。
通过分子对接模拟研究,刘兆鹏课题组推测,LL01分子中的酰胺基团有可能作用于α β微管蛋白交界处,形成一个新结合区,如下图所示:
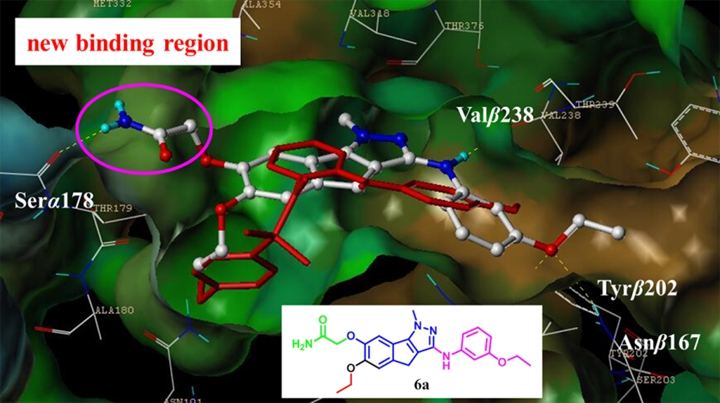
最新研究表明,LL01不是P-糖蛋白的作用底物,对P-gp过表达的肿瘤细胞有效,对紫杉醇耐药的肿瘤细胞也具有同等的抑制作用。作为具有开发前景的抗肿瘤候选分子,相关的临床前药学研究正在展开。
该研究成果在药化领域顶级期刊《Journal of Medicinal Chemistry》上发表,第一作者为山东大学药学院的硕士研究生刘晏娜和王静静同学,通讯作者为刘兆鹏教授和郭秀丽教授。
该研究工作得到了国家自然科学基金委(81573275)的资助。
http://pubs.acs.org/doi/abs/10.1021/acs.jmedchem.6b00071
原文:Design, Synthesis, and Biological Evaluation of 1-Methyl-1,4-dihydroindeno[1,2-c]pyrazole Analogues as Potential Anticancer Agents Targeting Tubulin Colchicine Binding Site.
J. Med. Chem., 2016, 59, 5341-5355, DOI: 10.1021/acs.jmedchem.6b00071
