四氢异喹啉-7-酰胺类选择性DDR1小分子抑制剂设计及应用研究
盘状结合域受体(Discoidin Domain Receptors,DDRs)因其独特的细胞外N末端盘状受体结合域而得名,是以胶原蛋白为信号分子的跨膜受体酪氨酸激酶,主要介导胶原蛋白引起的细胞增殖、粘附、迁移及肿瘤细胞侵袭和转移。DDRs家族包含DDR1和DDR2两个成员蛋白。DDRs的过度表达或激活与炎症发生、发展以及肿瘤侵袭、转移等过程密切相关,是开发治疗恶性肿瘤和纤维化、动脉粥样硬化等炎症相关疾病的潜在新靶标。目前的DDRs抑制剂存在选择性较差或活性较弱等缺陷,迫切需要高选择性抑制剂作为工具来研究其作为药物靶标的可能性。
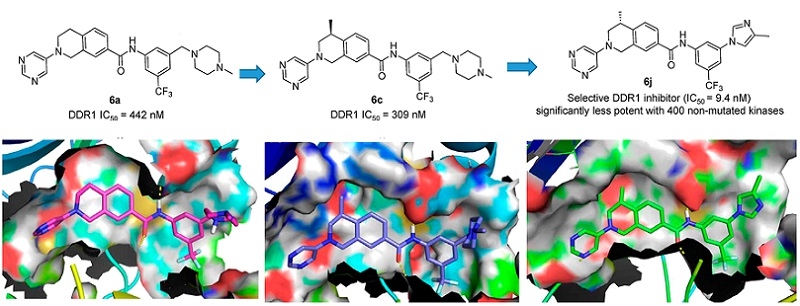
近日,中国科学院广州生物医药与健康研究院丁克教授(现任暨南大学药学院院长)研究团队携手第四军医大学苏金课题组及牛津大学Alex Bullock博士等采用基于结构的药物设计策略,成功设计合成了取代四氢异喹啉类分子作为全新的的特异性DDR1抑制剂。进而,通过结构生物学研究技术阐明了该类抑制剂与DDR1蛋白的结合模式。其中代表化合物6j对DDR1蛋白有很好的结合亲和力(Kd = 4.7nM)及激酶抑制活性(IC50 =9.4 nM),而对其他400种非突变型激酶都表现出良好的选择性,是目前已知特异性最强的DDR1抑制剂。同时,化合物6j还展示出良好的药代动力学性质,并在博莱霉素诱导的小鼠肺纤维化模型中表现出优良的治疗作用。
该项研究不仅为后续针对该药物靶点的创新药物开发提供了活性和特异性强的先导分子,也为DDR1的生物学功能研究提供了优异的探针分子。另外,该研究还首次证实DDR1小分子抑制剂可用于肺纤维化疾病的治疗,为该疾病的治疗提供了新的思路。鉴于该项成果的创新型和潜在应用价值,它被药物化学权威期刊Journal of Medicinal Chemistry选作封面进行重点推荐。本研究得到国家自然基金、广东省和广州市等的资金资助。
http://pubs.acs.org/doi/abs/10.1021/acs.jmedchem.6b00140
原文:Structure-Based Design of Tetrahydroisoquinoline-7-carboxamides as Selective Discoidin Domain Receptor 1 (DDR1) Inhibitors
J. Med. Chem., 2016, 59, 5911-5916, DOI: 10.1021/acs.jmedchem.6b00140
