手性化合物大搜查之“一点都不能少”:金属中心手性(中)
上回我们简要介绍了四面体型金属中心手性配合物(点此阅读相关),今天我们再接着聊一聊八面体型金属中心手性配合物的性质与应用。
八面体型金属中心化合物:通常情况下,6配位的过渡金属配合物会呈八面体型,而根据配体的不同又可以分为两类:半三明治型和线性多齿配体配位型。
半三明治型金属配合物特指其中一个配体具有芳香性,如茂基和苯基。理论上认为,芳香配体占据了6配位金属的一个面(即占据了3个可能的配位点),再加上3个其他的配体点,因此认为半三明治型属于八面体结构的一种(Figure 1)。

Figure 1. 半三明治型金属中心手性。图片来源:Chem. Soc. Rev., 2012, 41, 3153-3167
Cahn-Ingold-Prelog(CIP)序列法则同样适用于半三明治型金属中心的绝对构型归属,需要特别注意的是,在CIP规则下,一般认为芳香配体整体与金属中心具有配位作用,例如,茂基通常视为5个碳原子与金属等价配位,其配位分子量为60。常见的配体优先法则如下:I > Br > η6-C6H6 > η5-C5H5->η3-C3H3- > Cl > P(如PPh3)> O(如烷氧基)> N(如胺)>η1-C(如CH3)。如Figure 2所示,
除了茂基(η5-C5H5-)配体之外,过渡金属铼(Re)还有3个不同的配体,分别为C,N,P,根据上述的优先法则,金属中心的绝对构型确定为S。

Figure 2. 半三明治型Re配合物。图片来源:Chem. Soc. Rev., 2012, 41, 3153-3167
多种过渡金属,如Fe、Ru、Rh、Ir、Mo、Re等都可以用于合成半三明治型金属配合物。瑞士巴塞尔大学的Thomas R. Ward和Brunner教授等选取不饱和配位的单茂金属配合物,通过计算发现其非茂配体翻转的能垒不足15 kcal/mol(Figure 3)[1],再加上配体/金属配位作用的可逆性,导致金属手性中心极度易消旋,也决定了半三明治型唯金属中心手性配合物很难在不对称催化领域有所作为,而其中较成功的解决方案之一是辅以手性配体。
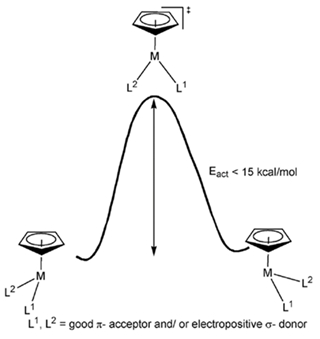
Figure 3. 单茂金属配合物的配体翻转能垒。图片来源:Organometallics, 1997, 16, 3207-3215
1994年,耶鲁大学的J. W. Faller教授小组设计合成了如Scheme 1所示的手性η3-茂基钼配合物(R)-21,可以与苯甲醛络合并进一步发生羰基-ene反应,得到手性高烯丙醇(>98% ee)[2]。
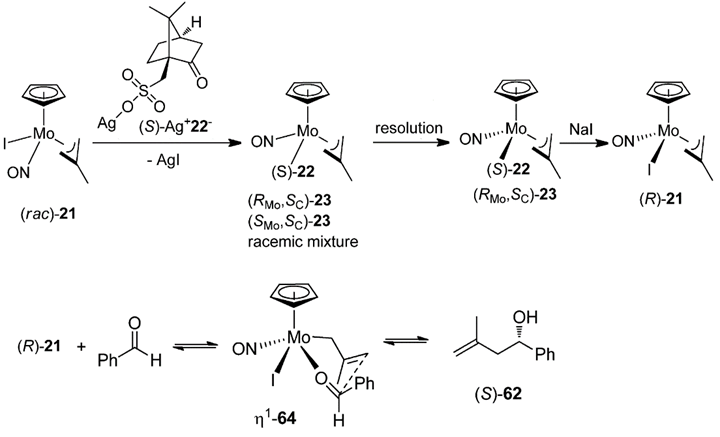
Scheme 1. η3-茂基钼配合物的手性拆分及其在不对称合成中的应用。图片来源:Organometallics, 1993, 12, 1434-1438
酰基单茂铁配合物,如(R)-65,是早期不对称合成常用的手性辅助基团[3],在正丁基锂的作用下,羰基官能团发生烯醇化,可以与合适的亲电试剂(如碘甲烷)发生反应,得到构型单一的α-官能化产物,最后可以在氧化条件下脱除手性辅基(Scheme 2)。

Scheme 2. 手性茂基酰基铁配合物的转化。图片来源:Pure Appl. Chem., 1988, 60 , 13-20
不对称环化反应也是半三明治型手性金属配合物“施展才华”的领域之一。2001年,J. W. Faller教授小组合成了手性伞花烃Ru配合物(RRu, Sc)-35,并用于催化的环戊二烯和丙烯醛的Diels-Alder反应,ee值可达99%(Scheme 3)[4]。
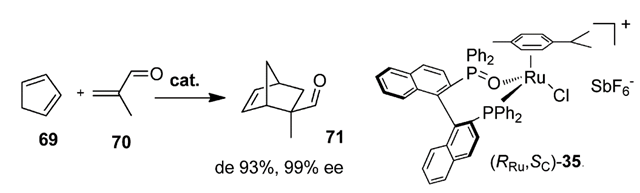
Scheme 3. 手性伞花烃Ru配合物催化的不对称Diels-Alder反应。图片来源:J. Am. Chem. Soc., 2001, 123, 2525-2529
2007年,西班牙萨拉戈萨大学(Universidad de Zaragoza)的Daniel Carmona和M. Plilar Lamata教授小组合成了基于手性双膦配体的茂基Rh和Ir配合物(Figure 4),并尝试用于催化α,β-不饱和醛和硝酮的[3+2]环化反应,发现铱催化的反应普遍得到高于铑催化剂的对映选择性(Scheme 4)[5]。
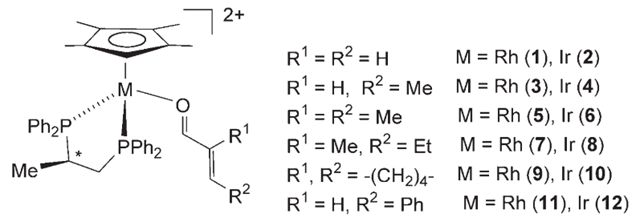
Figure 4. 含有手性双膦配体的茂基Rh和Ir配合物。图片来源:Adv. Synth. Catal., 2007, 349, 1751-1758
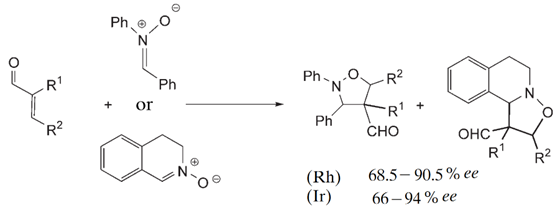
Scheme 4. 手性茂基Rh和Ir化合物催化的不对称[3+2]环化反应。图片来源:Adv. Synth. Catal., 2007, 349, 1751-1758
日本古屋大学的诺贝尔化学奖获得者R. Noyori教授也曾发展了系列手性伞花烃Ru配合物(Figure 5),用于酮类化合物的高对映选择性转移氢化反应[6];中科院北京化学所的范青华教授和香港理工大学的陈新滋院士合作发现,在离子液中可以实现喹啉的高效不对称氢化,ee值97-99%(Scheme 5)[7]。

Figure 5. Noyori教授发展的手性伞花烃Ru配合物。图片来源:Angew. Chem. Int. Ed., 2002, 41, 2008-2022
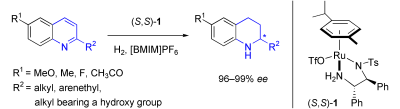
Scheme 5. 手性伞花烃Ru配合物催化的喹啉不对称氢化。图片来源:Angew. Chem. Int. Ed., 2008, 47, 8464-8467
半三明治型金属配合物是八面体型金属中心手性的重要组成部分,其中唯金属中心手性的合成研究较多,但是多数常温下不稳定,易消旋,限制了其在不对称催化领域的应用;辅以手性配体的半三明治型金属配合物可以作为手性Lewis酸催化含杂原子(O、N等)底物的不对称转化,但是反应类型依然很有限。
另一种八面体构型金属配合物具有多齿线性配体,近几年涌现出很多具有代表性的结构,并在不对称催化领域应用越来越广。预知后事如何,且听下回分解。
参考文献:
1. Geometry of Coordinatively Unsaturated Two-Legged Piano Stool Complexes with 16 Valence Electrons: A Theoretical Study. Organometallics, 1997, 16, 3207-3215
http://pubs.acs.org/doi/abs/10.1021/om9700369
2. Resolution of CpMo(NO)X(.eta.3-2-methallyl) complexes and their enantioselective reactions with an aldehyde. Organometallics, 1993, 12, 1434-1438
http://pubs.acs.org/doi/abs/10.1021/om00028a070
3. Asymmetric synthesis via the iron chiral auxiliary [(η5-C5H5)Fe(CO)(PPh3). Pure Appl. Chem., 1988, 60, 13–20
https://www.iupac.org/publications/pac/60/1/0013/index.html
4. An Application of Electronic Asymmetry to Highly Enantioselective Catalytic Diels−Alder Reactions. J. Am. Chem. Soc., 2001, 123, 2525-2529
http://pubs.acs.org/doi/abs/10.1021/ja003528c
5. Asymmetric 1,3-Dipolar Cycloaddition Reaction between α,β-Unsaturated Aldehydes and Nitrones Catalyzed by Well-Defined Iridium or Rhodium Catalysts. Adv. Synth. Catal., 2007, 349, 1751-1758
http://onlinelibrary.wiley.com/doi/10.1002/adsc.200700010/abstract
6. Asymmetric Catalysis: Science and Opportunities (Nobel Lecture). Angew. Chem. Int. Ed., 2002, 41, 2008-2022
7. Hydrogenation of Quinolines Using a Recyclable Phosphine-Free Chiral Cationic Ruthenium Catalyst: Enhancement of Catalyst Stability and Selectivity in an Ionic Liquid. Angew. Chem. Int. Ed., 2008, 47, 8464-8467
http://onlinelibrary.wiley.com/doi/10.1002/anie.200802237/abstract
(本文由岐黄柚子茶供稿)
