通过铑和手性质子梭共同催化的不对称N-H键插入反应合成α-烯基-α-氨基酸
α-烯基-α-氨基酸是一种自然界广泛存在的氨基酸,具有很多重要的生物活性。由于该类氨基酸具有烯基、氨基和羧基等多种官能团,非常便于转化,在有机合成中作为合成砌块被广泛应用。虽然人们已经发展出大量高效、高对映选择性的方法合成α-烷基和α-芳基取代的α-氨基酸,目前合成光学活性α-烯基-α-氨基酸的方法还很少,而且普遍存在底物谱窄、反应条件苛刻、催化剂用量高、副反应多等问题。因此发展高效、高选择性地合成α-烯基-α-氨基酸及其衍生物的新方法具有重要意义。
α-烯基重氮酯对N-H键的插入反应是合成α-烯基-α-氨基酸及其衍生物的潜在方法,但是由于缺少有效催化剂,该反应的高对映选择性转化一直没有实现。此外,由于重氮烯基部分容易发生环丙烷化、重排等副反应,该反应往往比较复杂,收率普遍很低。南开大学朱守非、周其林等发展了手性螺环磷酸作为质子梭催化剂,首次通过对金属催化反应活性中间体质子转移过程的直接控制,实现反应的手性诱导。此前该课题组使用手性质子梭催化剂成功实现了铑催化α-重氮化合物对N-H键、S-H键和芳环C-H键的不对称插入反应,开辟了卡宾插入反应的全新手性诱导模型(Angew. Chem. Int. Ed.2011, 50, 11483; Chem. Sci. 2014, 5, 1442; Angew. Chem. Int. Ed.2014, 53, 3913,J. Am. Chem. Soc.2015, 137, 8700)。
最近,该课题组进一步使用铑和手性质子梭共同催化的体系,实现了首例α-烯基重氮酯对N-H键的高对映选择性插入反应。手性质子梭催化剂通过叶立德中间体质子转移过程的直接控制实现了高效的不对称诱导,并且抑制了副反应,显著提高了收率。该反应具有底物谱广、催化剂活性高(催化剂用量在0.3 mol%时不影响反应结果,转化频率达到6000 /h)、副反应少,产率高等特点,成为合成α-烯基-α-氨基酸及其衍生物最高效的方法之一。该研究进一步显示了手性质子梭催化剂在含有质子转移关键步的有机反应中手性控制的独特优势,和其在不对称合成中的广阔应用前景。
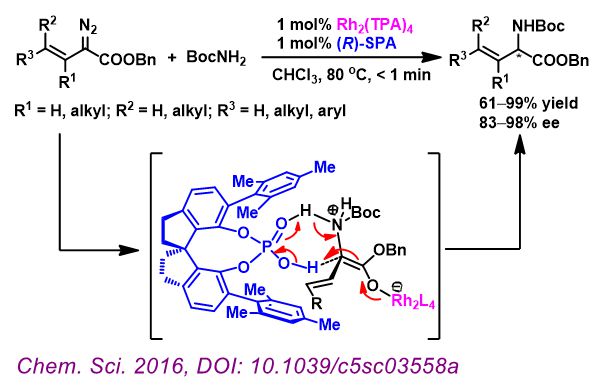
相关成果发表在《Chem. Sci.》( Chem. Sci., 2016, DOI: 10.1039/c5sc03558a)。
http://pubs.rsc.org/en/Content/ArticleLanding/2016/SC/C5SC03558A
原文标题:Enantioselective synthesis of α-alkenyl α-amino acids via N-H insertion reactions
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!




























 京公网安备 11010802027423号
京公网安备 11010802027423号