手性醛催化甘氨酸酯的不对称活化
在过去近20年时间里,有机催化领域得到迅速的发展。手性有机催化剂及其活化模式的开发为高对映体富集型手性分子的获得提供了可靠的方法。在不对称催化方法学发展的过程中,每一类新型催化剂或者活化模式的发现都可能为实现新的有机化学转化、合成结构新颖的手性化合物提供指导思路。同时,对于那些使用已知方法难以有效活化的底物,新催化剂和新活化模式的开发显得尤为重要。
西南大学化学化工学院的郭其祥教授(点击查看介绍)课题组一直致力于不对称合成方法学的开发及应用研究。2014年,郭其祥课题组首次提出了“基于亚胺活化机制的手性醛催化”策略:醛催化剂与伯胺类化合物形成亚胺中间体,通过亚胺活化机制形成活性α-亚胺碳负离子,继而进攻亲电试剂(E+),利用亚胺形成的可逆性原位解离生成含有游离氨基的手性胺,从而实现手性醛催化伯胺类化合物的不对称直接α-官能化反应(图1)。他们在该策略的指导下实现了氨基丙二酸酯与3-吲哚甲基醇的不对称烷基化反应(Chem. Sci., 2014, 5, 1988)(图2)。
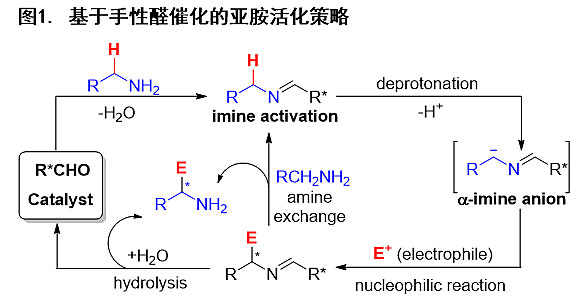
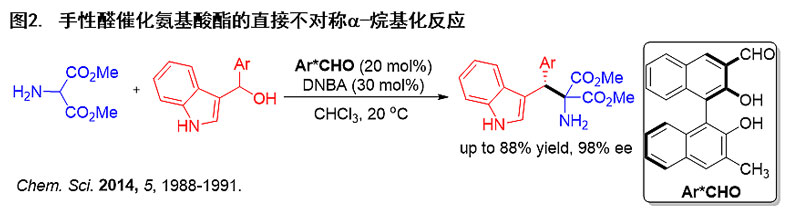
在这一启发性的工作之后,他们应用该策略实现了活性较低的伯胺类化合物的不对称活化,于最近取得了突破性进展。该课题组通过合理的设计,合成了一类更为高效的新型手性醛催化剂,将其用于甘氨酸酯的不对称活化,实现了手性醛催化甘氨酸酯对α,β-不饱和酮的不对称亲核加成/环化反应。相关工作在J. Am. Chem. Soc.上发表(图3)。

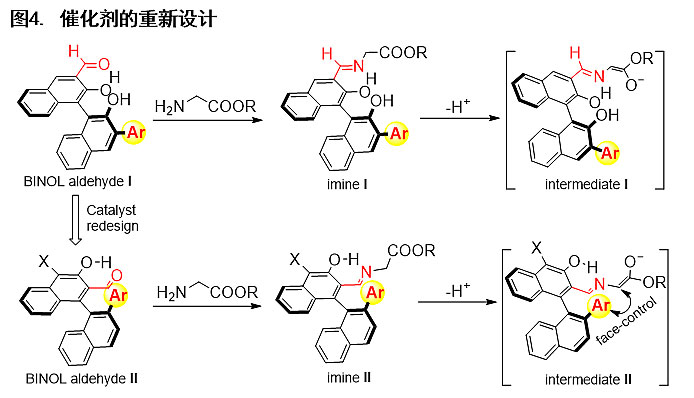
作者首先采用第一代手性醛催化剂BINOL aldehyde I对模板反应进行了尝试,但仅以中等的收率和对映选择性得到目标产物Δ(1)-吡咯啉。他们认为这可能是由于催化剂的催化位点(-CHO)和位阻基团(-Ar)均离手性中心较远,从而导致手性诱导效果较差。因此,作者对催化剂进行了重新设计:(1)将催化位点和位阻基团由3,3′位转移到离手性中心更近的2,2′位;(2)在催化剂的4位引入吸电子基团,以增加催化剂的活性。基于以上思考,作者合成了一系列新型的手性醛催化剂BINOL aldehyde II(图4),并将该类催化剂用于催化模板反应。结果表明,其催化活性和手性诱导能力均有了显著提高。
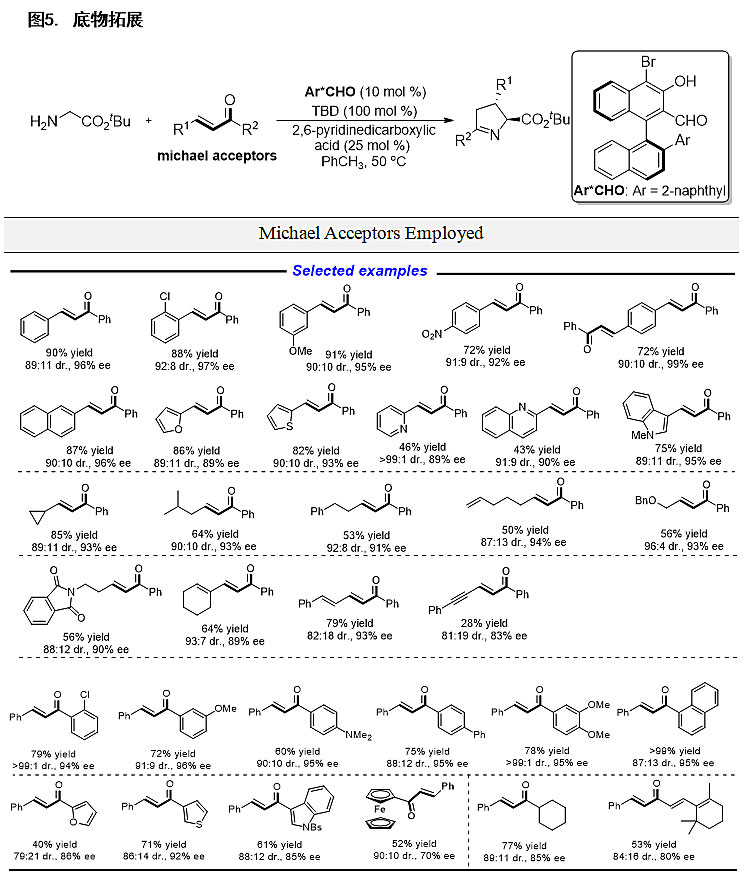
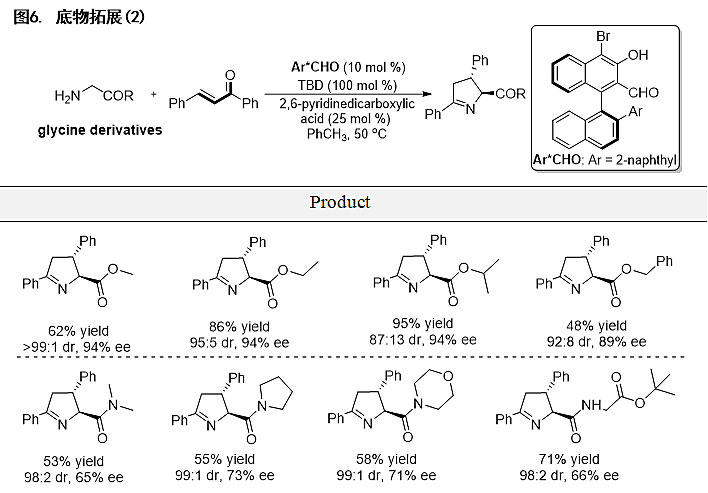
经过进一步的条件筛选和优化,他们得到最优的反应条件,并在该条件下对底物的适用范围进行考察。该催化体系具有非常广泛的底物适用性(>70 examples),对于各种取代基修饰的苯基、杂芳香基、烷基、烯基以及炔基取代的α,β-不饱和酮均具有很好的反应活性和立体选择性,对于醚键和酰胺键也具有一定的官能团兼容性(图5)。值得一提的是,作者还首次实现了醛催化甘氨酸衍生的酰胺和二肽的不对称活化,以中等的收率和对映选择性获得相应的目标产物,展现了醛催化在实现甘氨酸衍生的多肽结构修饰方面的潜力(图6)。
为了更加深入研究反应的历程,作者还与第三军医大学的欧阳勤教授合作,通过密度泛函理论(DFT)计算研究了反应可能的过渡态和反应立体选择性的控制及质子转移过程。计算结果表明,手性醛催化剂作为双功能催化剂,3位的酚羟基与相邻醛基之间的氢键对于降低亚胺形成和亲核加成过程中质子转移的能垒起着非常重要的作用(图7)。

郭其祥教授和欧阳勤教授为该论文的共同通讯作者,西南大学的博士生文巍和硕士研究生陈磊为共同第一作者。该工作得到国家自然科学基金(21472150)和重庆市科技创新领军人才支持计划项目的资金支持。
小结
郭其祥教授课题组继2014年实现了手性醛催化氨基丙二酸酯的活化之后,再次实现了低活性甘氨酸酯及甘氨酰胺α-C-H键的不对称活化。期待这一活化模式在催化伯胺化合物的不对称α-官能化方面取得新的研究进展。
该论文作者为:Wei Wen, Lei Chen, Ming-Jing Luo, Yan Zhang, Ying-Chun Chen, Qin Ouyang and Qi-Xiang Guo
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Chiral Aldehyde Catalysis for the Catalytic Asymmetric Activation of Glycine Esters
J. Am. Chem. Soc., 2018, 140, 9774, DOI: 10.1021/jacs.8b06676
导师介绍
郭其祥
http://www.x-mol.com/university/faculty/13987
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!



























 京公网安备 11010802027423号
京公网安备 11010802027423号