天然产物生物合成与合成生物学:双环霉素的生物合成与体外酶催化合成
2,5-二酮哌嗪(2,5-Diketopiperazines, DKPs)天然产物的核心骨架由两种氨基酸缩合并环化而成,是自然界最小的环肽衍生物。DKP骨架具有较强的刚性,不易被肽酶水解,分子中存在的氢键供体和受体基团有利于与靶标形成相互作用。在DKPs环外引入额外的环,有助于进一步提高分子在构象水平上的刚性,从而对靶标蛋白具有更高的选择性。一些DKPs天然产物还具有更加复杂的桥环结构(Bridged structure),如双环霉素(Bicyclomycin, BCM)具有自然界稀少的[4,2,2]-氧杂桥环二酮哌嗪骨架。
双环霉素具有显著的抗革兰氏阴性菌活性,且作用靶点非常特殊,是已知的唯一来源于天然产物的转录终止因子Rho蛋白的抑制剂。近年来的研究发现,该化合物与一些抗菌药物(如四环素类、氯霉素、利福霉素类等)的联合使用对包括一些临床耐药的革兰氏阴性菌具有协同致死效应,被认为有可能为克服革兰氏阴性菌的耐药性问题提供一条新的思路。作为一种具有桥环三维结构、脂肪链被高度氧化修饰的活性天然产物,双环霉素引起有机合成和生物合成领域的共同关注,对其进行体外酶催化合成研究,不仅有助于为这类自然界稀有的天然产物带来结构多样性,获得新型抗耐药菌药物前体,还能够为分子合成提供中链氧杂桥环构筑的新途径和惰性C-H键活化的新方法。
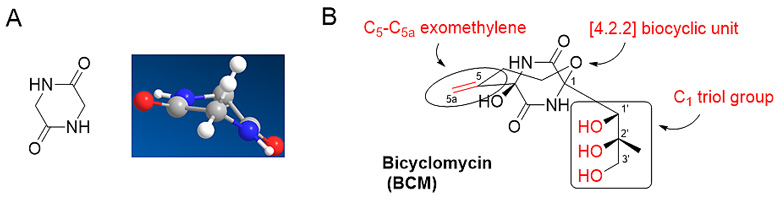
图1. 2,5-二酮哌嗪骨架(A)和双环霉素(B)的化学结构
近日,中国科学院上海有机化学研究所的唐功利研究员(点击查看介绍)团队首次实现了双环霉素的体外酶催化合成,阐明了双环霉素的完整生物合成途径,为氧杂桥环二酮哌嗪类化合物的合成生物学研究奠定了基础,相关工作主要由该团队的孟松和潘海学博士完成。
该团队采用在体外重构所有酶催化反应的策略来研究双环霉素的生物合成路径。在他们首次发现的BCM合成路径中共包含7种酶:1种环二肽合酶BcmA、5种非血红素铁依赖的双加氧酶BcmB/C/E/F/G和1种细胞色素P450单加氧酶BcmD。研究人员从环二肽合酶出发,对不同酶的功能进行了逐步、逐个验证,并分离鉴定了几乎所有酶催化中间的产物,最终成功地在体外重现了完整的双环霉素生物合成途径,同时也阐明了该途径中所有酶的催化功能。双环霉素的生物合成过程包括连续多步惰性C-H键的活化(BcmE-C-G-B-D-F)以及在C-H键活化(BcmE-C-G)的基础上一步脱氢-环氧化-氧杂桥环形成的过程(BcmB)。
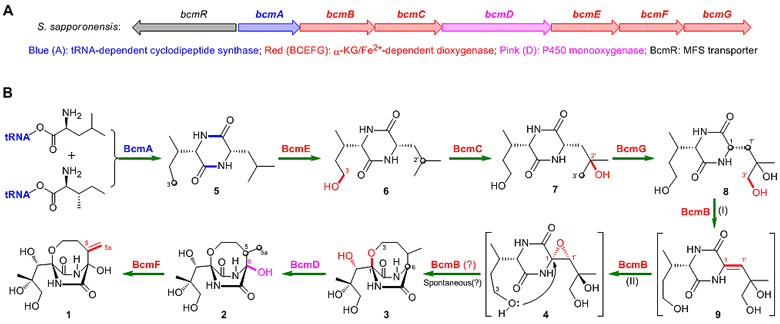
图2. 双环霉素的生物合成基因簇(A)和完整的生物合成途径(B)
在全面解析生物合成途径的基础上,他们以化学合成的环二肽5为底物,采用分步加酶的方式,一锅法实现了双环霉素酶催化的全合成,为进一步酶催化的高效全合成、类似物的制备及酶反应机制的深入探讨创造了条件。这一成果近期发表在Angewandte Chemie International Edition 上。
该论文作者为:Song Meng, Wei Han, Juan Zhao, Xiao-Hong Jian, Hai-Xue Pan, Gong-Li Tang
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

A Six-Oxidase Cascade for Tandem C−H Bond Activation Revealed by Reconstitution of Bicyclomycin Biosynthesis
Angew. Chem. Int. Ed., 2018, 57, 719, DOI: 10.1002/anie.201710529
导师介绍
唐功利
http://www.x-mol.com/university/faculty/15570
课题组链接
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!



























 京公网安备 11010802027423号
京公网安备 11010802027423号