高效捕获和灵敏检测循环肿瘤细胞的纳流控新方法
癌症是造成人类死亡的主要原因之一,据癌症统计数据显示,癌症引起的死亡90%以上都是由癌转移引起。在肿瘤转移扩散过程中进入外周血循环的肿瘤细胞被称为循环肿瘤细胞(CTCs)。当CTCs从原发部位脱落,进入外周血循环,转移至宿主器官部位,最终导致了癌症的相关死亡。因此,CTCs的早期发现,对癌症早期诊断具有重要意义。但是,由于CTCs在早期癌症患者的外周血中数量极少,大约每106~107个白细胞中只有一个CTC,因此对CTCs的分离和检测具有极大的挑战性。
近日,中国药科大学王琛(点击查看介绍)课题组和南京大学夏兴华(点击查看介绍)教授课题组合作,发展了一种基于阵列离子-纳米通道复合结构和电化学检测技术,对CTCs进行高效捕获和灵敏检测的纳流控新方法(图 1)。该工作首先在离子通道表面修饰适体探针分子,通过特异性识别CTCs膜上的特定蛋白,实现CTCs的高选择性捕获。被捕获的CTCs显著影响离子-纳米复合结构的物质传输性质,因此采用原位电化学技术,可实现CTCs的高效捕获和灵敏检测(图2A/B)。捕获的CCRF-CEM细胞采用全能核酸酶消化裂解而释放。通过细胞荧光染色图(图2C/D)分析可知,在捕获前后细胞活性变化不大,即捕获过程对细胞损伤较小,有利于细胞的后期研究。该研究提供了一种简单、灵敏、无标记的CTCs捕获和检测新方法,在癌症的早期诊断和临床治疗方面具有重要的应用价值。

图 1. (A)细胞捕获、检测与释放的装置示意图;(B)细胞在离子-纳米通道复合结构上捕获和释放过程的示意图;(C)细胞捕获和释放前后复合结构的物质传输性质。
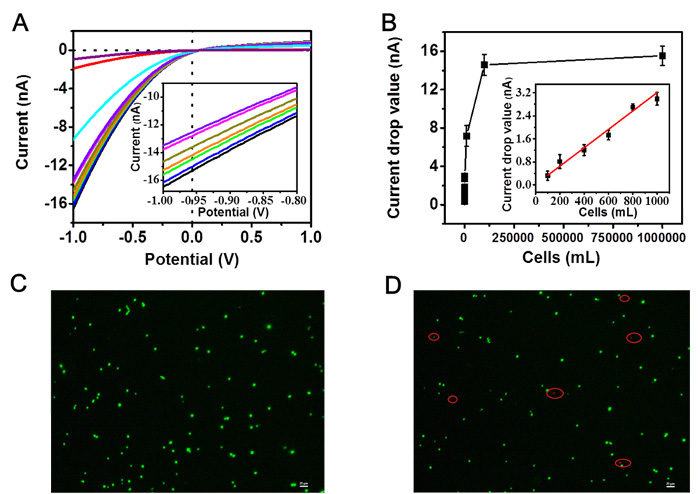
图 2. (A)不同CTCs浓度下离子-纳米通道复合的i-v曲线图;(B)不同CTCs浓度下离子-纳米通道复合在-1V电压处电流值的绝对值。(C)CTCs捕获前溶液中细胞的AO /PI双染色的荧光显微图;(D)CTCs经全能核酸酶消化释放后溶液中细胞的AO /PI双染色的荧光显微图。
该研究成果近期发表于美国化学会期刊Analytical Chemistry,中国药科大学硕士研究生曹静为该论文的第一作者。该项目得到国家自然科学基金和江苏省自然科学基金的支持。
该论文作者为:Jing Cao, Xiao-Ping Zhao, Muhammad Rizwan Younis, Zhong-Qiu Li, Xing-Hua Xia,* Chen Wang*
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Ultrasensitive Capture, Detection, and Release of Circulating Tumor Cells Using a Nanochannel–Ion Channel Hybrid Coupled with Electrochemical Detection Technique
Anal. Chem., 2017, 89, 10957-10964, DOI: 10.1021/acs.analchem.7b02765
王琛博士简介
王琛,中国药科大学理学院副教授。2011年于南京大学取得分析化学博士学位;2012年至2016年,在南京大学物理系从事博士后研究;2016年至2017年在美国麻省理工学院材料科学学院进行访学研究。主要研究方向为微纳流控分析新方法研究。已在ACS Nano, Anal. Chem. Lab Chip, Chem. Eur J, ACS Appl. Mater. Interfaces, Electrochem. Commun. 等刊物发表论文30余篇。
王琛
http://www.x-mol.com/university/faculty/48468
夏兴华
http://www.x-mol.com/university/faculty/11579
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!



























 京公网安备 11010802027423号
京公网安备 11010802027423号